
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:填空题
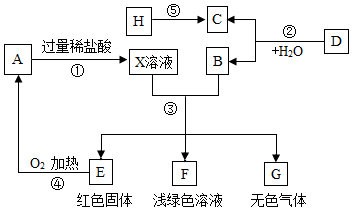
 甲、乙、丙和A-F是初中化学常见物质,如图所示是它们之间的相互转化关系,(部分反应条件及反应物、生成物已略去).已知:①甲、乙、丙均为单质,A-F均为化合物;②B常温下为液体,其组成比A多一种元素;③D是铁锈的主要成分.
甲、乙、丙和A-F是初中化学常见物质,如图所示是它们之间的相互转化关系,(部分反应条件及反应物、生成物已略去).已知:①甲、乙、丙均为单质,A-F均为化合物;②B常温下为液体,其组成比A多一种元素;③D是铁锈的主要成分.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
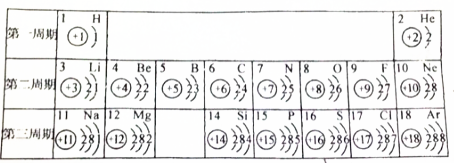
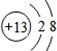 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 日常生活中煮沸水能降低水的硬度 | |
| B. | 可用灼烧法区分羊毛与合成纤维 | |
| C. | 可用3%~5%碳酸氢钠溶液处理皮肤上的少量硫酸 | |
| D. | 可用带火星的木条检验空气、O2、CO2 |
查看答案和解析>>
科目: 来源: 题型:解答题
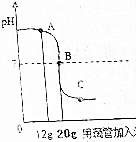 某兴趣小组为测定提纯后的碳酸钠的含量,进行如下实验:
某兴趣小组为测定提纯后的碳酸钠的含量,进行如下实验:查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com