
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
 化学元素与我们的健康是息息相关的,碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3),如图所示,超市销售的一种加碘盐标签上的部分文字说明.
化学元素与我们的健康是息息相关的,碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3),如图所示,超市销售的一种加碘盐标签上的部分文字说明.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
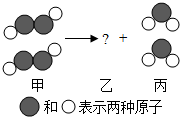
| A. | 该反应是化合反应 | B. | 甲是有机物 | ||
| C. | 甲的相对分子质量为34g | D. | 乙由一种元素组成 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用食盐制纯碱需要含碳、氧元素的物质 | |
| B. | (1)中析出晶体后剩余溶液只有一种溶质 | |
| C. | 氨盐水比食盐水更易吸收二氧化碳 | |
| D. | 碳酸氢钠比碳酸钠受热更易分解 |
查看答案和解析>>
科目: 来源: 题型:填空题
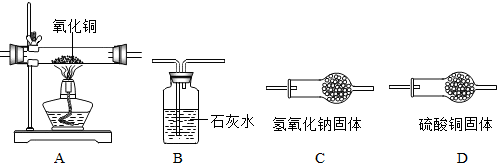
查看答案和解析>>
科目: 来源: 题型:解答题
 阅读下列材料,回答相关问题:
阅读下列材料,回答相关问题:查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com