
科目: 来源: 题型:填空题
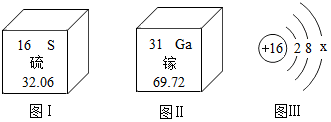
查看答案和解析>>
科目: 来源: 题型:解答题
 FeCl3溶液能对过氧化氢的分解起催化作用,某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响.
FeCl3溶液能对过氧化氢的分解起催化作用,某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响. | 30% H2O2溶液的体积(mL) | 2% FeCl3溶液的体积(mL) | 加入H2O的体积(mL) | 反应的时间(min) | 生成O2的体积(mL) |
| 1 | 5 | x | 20 | 5 | V1 |
| 2 | 10 | 3 | 15 | y | V2 |
查看答案和解析>>
科目: 来源: 题型:解答题


查看答案和解析>>
科目: 来源: 题型:解答题
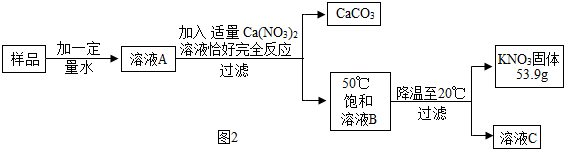
 溶解度是解决溶液相关问题的重要依据.
溶解度是解决溶液相关问题的重要依据.| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | KNO3 | 31.6 | 45.8 | 85.5 | 100 | 169 |
| K2CO3 | 110 | 114 | 121 | 126 | 139 | |
查看答案和解析>>
科目: 来源: 题型:解答题
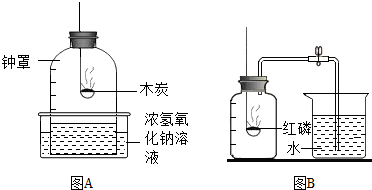
| 组别 | 1 | 2 | 3 | 4 | 5 | 6 |
| 进入集气瓶中水的体积/mL | 30 | 21 | 19 | 22 | 15 | 20 |
查看答案和解析>>
科目: 来源: 题型:解答题
 根据图示完成相关问题:
根据图示完成相关问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 能使紫色石蕊试液变为红色 | B. | 能与氢氧化钠溶液反应生成水 | ||
| C. | 能与硝酸银溶液反应生成白色沉淀 | D. | 能与锌反应生成氢气 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 化学计量数a与b之和一定等于c与d之和 | |
| B. | 若A和C都是盐,则该反应一定是复分解反应 | |
| C. | 反应物A和B的质量比一定等于生成物C和D的质量比 | |
| D. | 若取xgA和xgB反应,生成C和D的质量总和不一定是2xg |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com