
科目: 来源: 题型:解答题
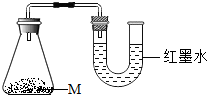 糕点包装袋中常见的保鲜剂组成为还原性铁粉、氯化钠、炭粉等.某化学兴趣小组为了探究铁粉的作用,设计了如下实验:
糕点包装袋中常见的保鲜剂组成为还原性铁粉、氯化钠、炭粉等.某化学兴趣小组为了探究铁粉的作用,设计了如下实验:| 实验 | M成分 | 实验现象 |
| Ⅰ | 干燥的铁粉、炭粉和氯化钠的混合物 | U型管左、右两端液面相平 |
| Ⅱ | 用氯化钠的溶液浸泡的铁粉、炭粉 | U型管左端液面明显高于右端 |
| Ⅲ | 用水浸泡的铁粉和炭粉 | U型管左、右两端液面基本相平 |
| Ⅳ | 用氯化钠溶液浸泡的铁粉 | U型管左端液面略高于右端 |
查看答案和解析>>
科目: 来源: 题型:解答题
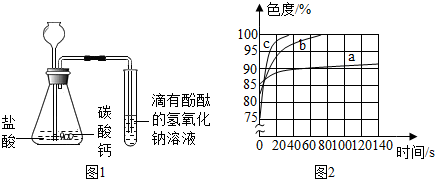
| 实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
| ①将NaOH溶液加热煮沸 | ①除去溶液中的氧气 | 溶液变红,过一会儿红色消失 | 甲同学猜想不正确(填“正确”或不正确”) |
| ②向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 | ②隔绝氧气 |
查看答案和解析>>
科目: 来源: 题型:解答题
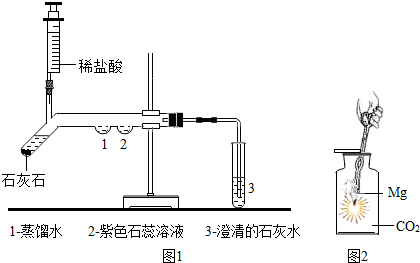
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
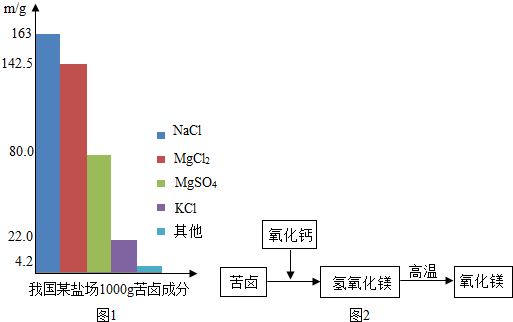
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com