
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
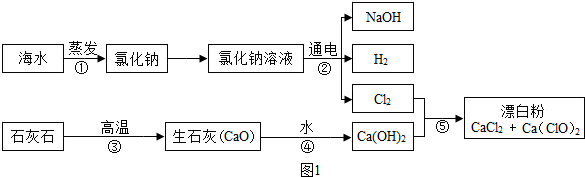
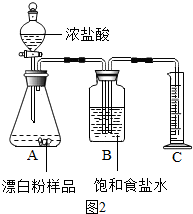
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,滴加足量的稀盐酸. | 有气体产生,气体使石灰水变浑浊. | 猜想2成立 |
| ②在上述反应后的试管中加少量品红溶液. | 红色变浅或消失. |
查看答案和解析>>
科目: 来源: 题型:解答题

| Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀的pH | 1.9 | 4.7 |
| 沉淀完全的pH | 3.2 | 6.7 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 利用沉降的方法,将硬水转化为软水 | |
| B. | 合理使用农药化肥,减少水污染 | |
| C. | 城市浇花草,使用喷灌、滴灌的方法 | |
| D. | 城建中实现雨污管道分离 |
查看答案和解析>>
科目: 来源: 题型:解答题
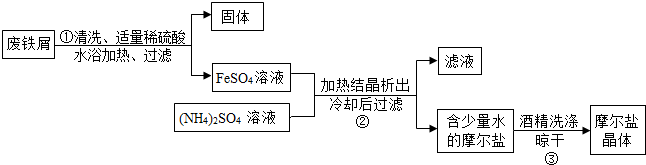
| 温度/℃ | FeSO4 | (NH4)2SO4 | FeSO4•(NH4)2SO4•6H2O |
| 10 | 20.0 | 73 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78 | 28.1 |
查看答案和解析>>
科目: 来源: 题型:选择题
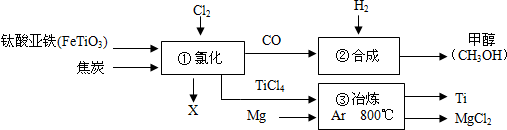
| A. | ③中氩气(Ar)作反应物 | |
| B. | 流程中的一氧化碳、钛酸亚铁和甲醇都是氧化物 | |
| C. | ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为7:1 | |
| D. | ①中反应为2FeTiO3+6C+7Cl2$\frac{\underline{\;一定条件\;}}{\;}$2x+2TiCl4+6CO,则x为FeCl2 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | ④ | B. | ③④ | C. | ①④ | D. | ②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com