
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
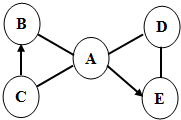 化学物质之间很多可相互反应或相互转化.相互关系如下图所示.
化学物质之间很多可相互反应或相互转化.相互关系如下图所示.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.07 | 17 Cl 氯 35.45 |
| A. | 失电子能力:Na>Al | B. | 镁和硅两种元素均属于非金属元素 | ||
| C. | 磷的相对原子质量是30.97 | D. | 得电子能力:S<Cl |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
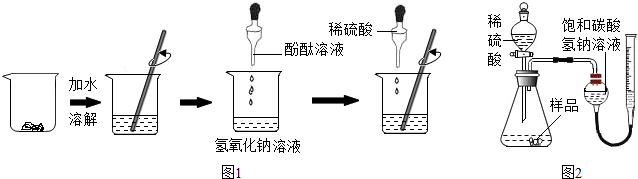
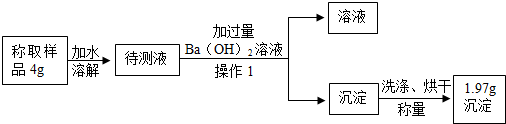
查看答案和解析>>
科目: 来源: 题型:填空题
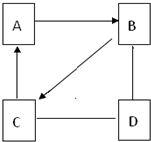 A、B、C、D是初中化学常见的物质,它们分别属于氧化物、酸、碱或盐中的一种,相互反应的关系如图(“-”表示相连的两种物质能发生化学反应,“→”表示转化关系,部分反应物或生成物省略).其中A、B、C含有两种相同元素,B可用于改良酸性土壤.请按要求回答下列问题:
A、B、C、D是初中化学常见的物质,它们分别属于氧化物、酸、碱或盐中的一种,相互反应的关系如图(“-”表示相连的两种物质能发生化学反应,“→”表示转化关系,部分反应物或生成物省略).其中A、B、C含有两种相同元素,B可用于改良酸性土壤.请按要求回答下列问题:查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com