
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验操作 | 预期现象 | 结论 |
| 步骤1: 向滤液中加入足量的氢氧化钡溶液 | 产生白色沉淀 | 猜想④成立 |
| 步骤2: 过滤,向白色沉淀中加入足量的稀盐酸 | 沉淀部分溶解,产生气泡 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验编号 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 25℃ | 二氧化锰 | 10mL 2%H2O |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O |

查看答案和解析>>
科目: 来源: 题型:解答题
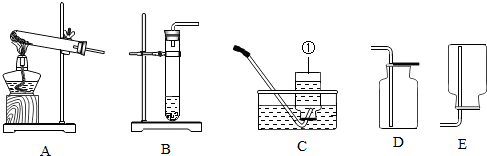
查看答案和解析>>
科目: 来源: 题型:解答题
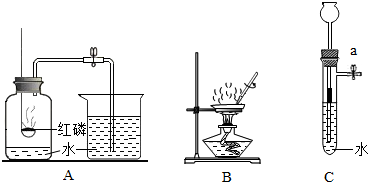
查看答案和解析>>
科目: 来源: 题型:解答题
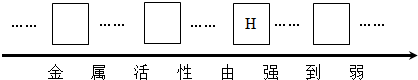
查看答案和解析>>
科目: 来源: 题型:解答题
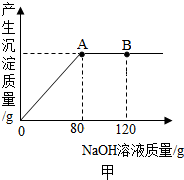 某同学欲利用单质铜制取Cu(OH)2,其设计方案如图所示:
某同学欲利用单质铜制取Cu(OH)2,其设计方案如图所示:
查看答案和解析>>
科目: 来源: 题型:解答题
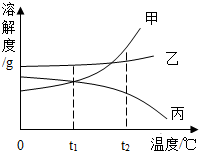 如图是甲、乙、丙三种物质的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液,请根据图中回答:
如图是甲、乙、丙三种物质的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液,请根据图中回答:查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com