
科目: 来源: 题型:解答题
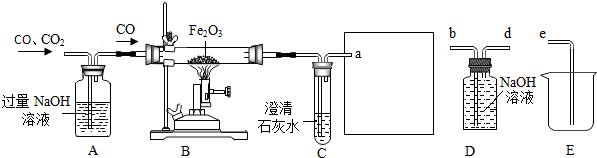
| 温度/℃ | 10 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/(g/100g水) | 64 | 85 | 138 | 203 | 285 | 376 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
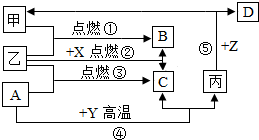 如图是初中化学中常见物质间的转化关系,其中甲、乙为气态单质,丙为固态单质;A、B、C均为氧化物,常温下B为液态.化合物D的水溶液呈浅绿色.
如图是初中化学中常见物质间的转化关系,其中甲、乙为气态单质,丙为固态单质;A、B、C均为氧化物,常温下B为液态.化合物D的水溶液呈浅绿色.查看答案和解析>>
科目: 来源: 题型:解答题
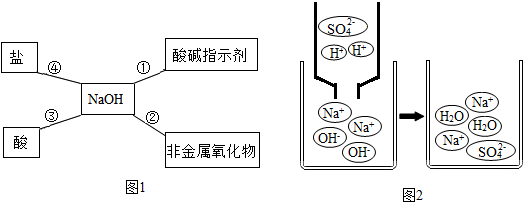
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 除去杂质的方法 |
| A | O2 | CO2 | 通过碱石灰 |
| B | Cu粉 | Fe粉 | 加入过量稀盐酸,过滤 |
| C | CO2 | CO | 通入氧气点燃 |
| D | FeCl2溶液 | CuCl2 | 加过量Fe粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题
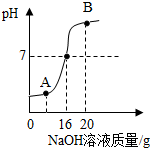 实验室测定一瓶稀硫酸中溶质的质量分数,取10g该待测液,向其中逐滴加入溶质质量分数为8%的氢氧化钠溶液,加入氢氧化钠溶液的质量与溶液pH的变化关系如图所示.请根据题意填空并计算:
实验室测定一瓶稀硫酸中溶质的质量分数,取10g该待测液,向其中逐滴加入溶质质量分数为8%的氢氧化钠溶液,加入氢氧化钠溶液的质量与溶液pH的变化关系如图所示.请根据题意填空并计算:查看答案和解析>>
科目: 来源: 题型:解答题
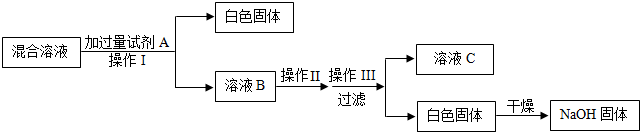
| 方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取样品少量于试管中,向其中加入足量的稀盐酸 | 产生气泡 | 白色物质是碳酸钠 |
| 方案2 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为氧化钠 |
| 方案3 | ①取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的氯化钙溶液 | 出现白色沉淀 | 白色物质是碳酸钠 |
| ②静置片刻,取上层清液于试管中,滴加酚酞(或硫酸铜)(要求:所填试剂属于不同类别) | 无明显现象 |
查看答案和解析>>
科目: 来源: 题型:解答题
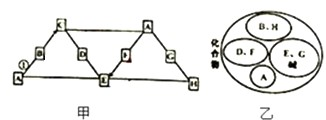
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com