
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
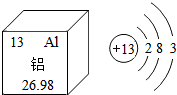 铝元素与人类关系密切.
铝元素与人类关系密切.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
| 金属 | Cr | Mg | Cu |
| 与盐酸反应现象 | 放出气泡速率缓慢 | 放出气泡速率较快 | 无明显现象 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
| 实验步骤 | 应得到的实验现象 | 结论与解释 |
| ①大理石和石灰石样本中都含有碳酸钙. ②花岗岩样本中不含碳酸钙. |
查看答案和解析>>
科目: 来源: 题型:解答题
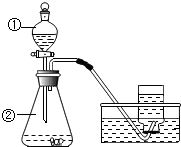 实验室制取气体时,首先要选择反应物,明确如何控制反应条件,然后确定气体发生和收集装置,还要考虑装置是否符合环保、安全等要求.请回答以下问题:
实验室制取气体时,首先要选择反应物,明确如何控制反应条件,然后确定气体发生和收集装置,还要考虑装置是否符合环保、安全等要求.请回答以下问题:查看答案和解析>>
科目: 来源: 题型:解答题
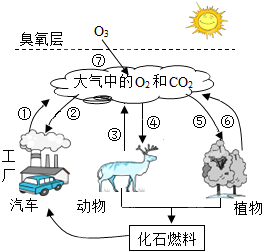 如图所示是自然界中氧气和二氧化碳的循环简图,请仔细读图,回答下列问题:
如图所示是自然界中氧气和二氧化碳的循环简图,请仔细读图,回答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题
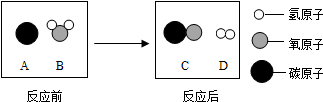
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com