
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 10% | B. | 20% | C. | 30% | D. | 40% |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该物质由5种元素组成 | |
| B. | 该物质中NH4+和SO42-的微粒个数比为1:2 | |
| C. | 该物质中铝元素的化合价为+3价 | |
| D. | 该物质中氢元素和硫元素的质量比是1:8 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 铁可以制成铁锤,是因为铁的硬度大 | |
| B. | 菜刀用完后要洗净抹干,是因为铁会生锈 | |
| C. | 铁可以制成铁丝,是因为它具有良好的延展性 | |
| D. | 铁锅上装有木质或塑料的手柄,因为铁能导电 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
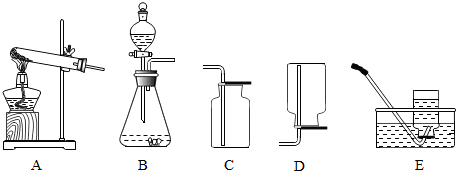
| 实验编号 | 硫酸溶液的浓度 (均取20mL) | 锌的形状 (均取1g) | 气体的体积(mL) (均收集3分钟) |
| A | 20% | 锌粒 | 31.7 |
| B | 20% | 锌片 | 50.9 |
| C | 30% | 锌粒 | 61.7 |
| D | 30% | 锌片 | 79.9 |
查看答案和解析>>
科目: 来源: 题型:解答题
 用科学方法认识物质
用科学方法认识物质
查看答案和解析>>
科目: 来源: 题型:解答题
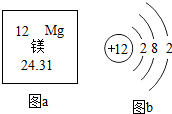 金属镁--未来的燃料
金属镁--未来的燃料查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com