
科目: 来源: 题型:解答题
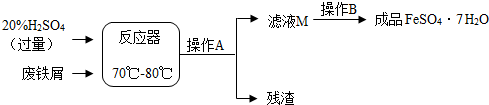
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | |
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 发展燃煤发电 | B. | 研究新能源汽车 | ||
| C. | 禁止焚烧秸秆 | D. | 加强建筑工地扬尘控制 |
查看答案和解析>>
科目: 来源: 题型:解答题
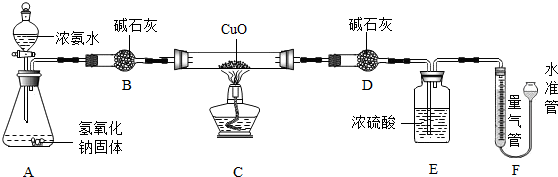
查看答案和解析>>
科目: 来源: 题型:解答题
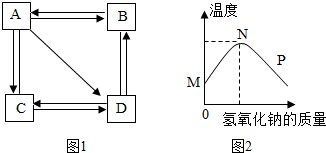

查看答案和解析>>
科目: 来源: 题型:解答题
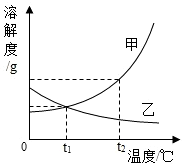 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.查看答案和解析>>
科目: 来源: 题型:解答题
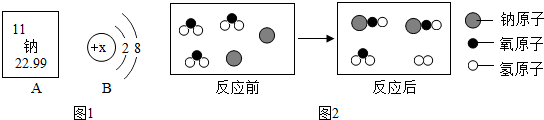
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 4 | B. | 3 | C. | 2 | D. | 1 |
查看答案和解析>>
科目: 来源: 题型:选择题
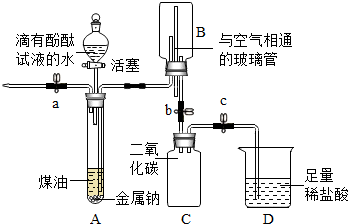 金属钠在空气中极易被氧化,常温下能与水剧烈反应生成氢氧化钠和氢气.化学兴趣小组同学在老师指导下设计了下图所示装置进行实验探究(支持装置已略去).已知:该装置气密性良好;煤油不与金属钠反应;煤油密度比水小且不溶于水.
金属钠在空气中极易被氧化,常温下能与水剧烈反应生成氢氧化钠和氢气.化学兴趣小组同学在老师指导下设计了下图所示装置进行实验探究(支持装置已略去).已知:该装置气密性良好;煤油不与金属钠反应;煤油密度比水小且不溶于水.| 步骤 | 操 作 | 现 象 |
| Ⅰ | 先打开a,再打开分液漏斗活塞.待大试管A中充满液体后,立即关闭a及分液漏斗活塞 | A中液体分层,油层在上.钠熔成银白色小球,在液体的界面处剧烈反应,产生大量气泡;下层溶液呈红色,并逐渐进入B中 |
| Ⅱ | 打开b,待B中部分溶液进入C中时关闭b,并打开a排气减压 | C中溶液仍呈红色 |
| Ⅲ | 打开止水夹c | D中溶液进入C中,产生气泡,溶液变为无色 |
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在CaCO3→CaO→Ca(OH)2→CaCO3的转化过程中钙元素质量保持不变 | |
| B. | 不能一步反应实现CuO→Cu(OH)2的相互转化 | |
| C. | 实现CO?CO2的相互转化,都只有一种途径 | |
| D. | 实现H2SO4→HCl和Ca(OH)2→NaOH的转化所发生反应的基本类型相同 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 分子可分为原子,而原子不可再分 | |
| B. | 金刚石和石墨物理性质有巨大差异,原因是其中碳原子的结构不同 | |
| C. | 水结冰体积变大时,水分子由运动到静止且水分子体积变大 | |
| D. | 空气是一种混合物,其中含有多种不同的分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com