
科目: 来源: 题型:解答题
| H | Na | Cl | O | K | Ca | Mg |
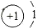 | 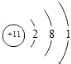 | 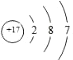 | 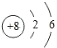 | 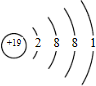 | 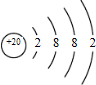 |  |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 一定含有C、H、O三种元素 | B. | 一定含有C、H元素不含有O元素 | ||
| C. | 一定含有C、H元素,可能含有O元素 | D. | 不能确定 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 冰水混合物 稀有气体 | B. | 清新的空气 液态氧气 | ||
| C. | 氮气 二氧化碳 | D. | 澄清的石灰水 清澈的泉水 |
查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:选择题
| 物质 | A | B | C | D |
| 反应前质量(g) | 20 | 20 | 20 | 20 |
| 反应后质量(g) | 20 | 30 | 未知 | 14 |
| A. | A物质可能是该反应的催化剂 | B. | 容器内发生了化合反应 | ||
| C. | 反应后容器内C的质量为16g | D. | 其化学方程式为:2C+3D═5B |
查看答案和解析>>
科目: 来源: 题型:解答题
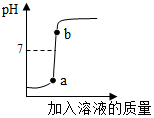 配制4%的氢氧化钠溶液200g,并用此溶液测定某硫酸溶液的溶质质量分数.
配制4%的氢氧化钠溶液200g,并用此溶液测定某硫酸溶液的溶质质量分数.查看答案和解析>>
科目: 来源: 题型:解答题
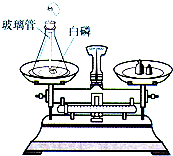 如图是测定白磷燃烧前后质量变化的实验,试回答下列问题:
如图是测定白磷燃烧前后质量变化的实验,试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com