
科目: 来源: 题型:解答题
| 实验步骤 | 现象 | 结论 |
| 取少量NaOH溶液样品于试管中,先滴加足量的CaCl2溶液,然后再滴加酚酞试液. | 有白色沉淀生成,酚酞溶液变为红色 | NaOH溶液部分变质 |
查看答案和解析>>
科目: 来源: 题型:解答题
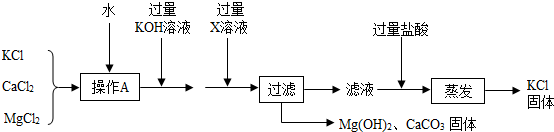
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:填空题
| 物质 | NaCl | NH4HCO3 | NH4Cl | NaHCO3 |
| 溶液度/g | 36.0 | 21.6 | 37.2 | 9.6 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 等于3g | B. | 大于或等于3g | C. | 不等于3g | D. | 不大于3g |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 20℃时,100g氯酸钾饱和溶液中含氯酸钾7.4g | |
| B. | 20℃时,氯酸钾在水中溶解7.4g,溶液达到饱和 | |
| C. | 100g水中最多溶解7.4g氯酸钾 | |
| D. | 20℃时,100g水中溶解7.4g氯酸钾,溶液达到饱和状态 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验目的 | 实验步骤 | 可能的实验现象 | 化学方程式和实验结沦 |
| 探究所用 澄清石灰 水是否变 质 | ①用一支试管另取少量原澄清石灰水②取稀硫酸与碳酸钠 反应制取CO2 ③将产生的气体通入所用澄清石灰水中 | 步骤③中现象为: 石灰水变浑浊,或未变浑浊 | 步骤②中反应方程式为: H2SO4+Na2CO3=Na2SO4+H2O+CO2↑ 步骤③可能的反应方程式略 实验结论:所用澄清石灰水没有变质,或所用澄清石灰水已变质 |
| 实验目的 | 实验步骤 | 实验现象 | 化.学方程式和实验结论 |
| 探究气体X中是否含有HCl气体 | 将气体X通入硝酸银溶液 | 有白色沉淀生成 | 反应方程式为:HCl+AgNO3=AgCl↓+HNO3 实验结论:气体X中含有HCl气体 |
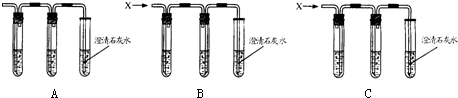
查看答案和解析>>
科目: 来源: 题型:选择题
| 实验操作 | 实验现象 | 实验结论 | |
| A | 将一根未打磨的铝条放入 硫酸铜溶液中 | 无紫红色固体析出 | 铝不如铜活泼 |
| B | 将带火星的木条伸入氧气中 | 木条复燃 | 氧气能支持燃烧 |
| C | 将CO通过灼热的氧化铜 | 黑色氧化铜变成红色 | CO具有可燃性 |
| D | 将氢氧化钠固体加入水中 | 溶液温度升高 | 该反应放热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com