
科目: 来源: 题型:选择题
| A. | 香烟烟气中有尼古丁等有毒物质,吸烟有害健康 | |
| B. | 绿色食品不含任何化学物质 | |
| C. | 天然物质都无毒无害 | |
| D. | 食用经甲醛水溶液浸泡过的水产品对人体有益 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| A | B | C | |
| 放入苹果起始时间 | 下午2:00 | 下午2:00 | 下午2:00 |
| 实验现象 | 下午2:03 苹果变色 | 下午2:09 苹果变色 | 下午2:19 苹果未变色 |
| A | B | |
| 进入水的体积 | 200mL | 42mL |
| 消耗气体的体积 | 50mL | 8mL |
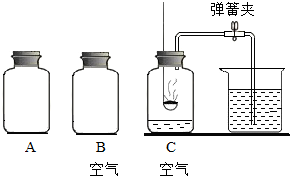
查看答案和解析>>
科目: 来源: 题型:解答题
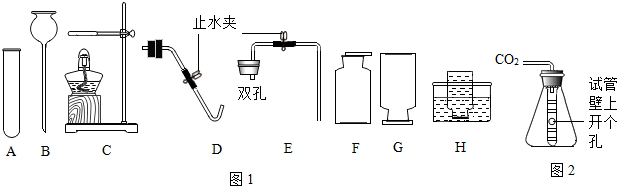
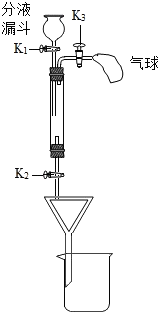 甲、乙两个实验小组利用如图装置(夹持装置已略去),做了一个兴趣实验,证明了二氧化碳与氢氧化钠的反应产物中有碳酸钠生成.他们的实验步骤如下:
甲、乙两个实验小组利用如图装置(夹持装置已略去),做了一个兴趣实验,证明了二氧化碳与氢氧化钠的反应产物中有碳酸钠生成.他们的实验步骤如下:查看答案和解析>>
科目: 来源: 题型:填空题
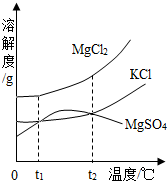 食盐在生活中具有广泛的用途.
食盐在生活中具有广泛的用途.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
 人的胃酸过多,会引起胃病.如图所示是某抗酸药标签上的部分文字.某同学为了测定该药中氢氧化铝的质量分数,进行如下操作:取一片药片(药片质量0.5g),研碎后加20mL蒸馏水,然后用质量分数为5%的盐酸至反应完全(其他成分不与盐酸反应),测定实验中反应掉的盐酸为6.0g.通过计算,判断该药片中氢氧化铝的含量是否达到标准以及该药片中氢氧化铝的质量分数.
人的胃酸过多,会引起胃病.如图所示是某抗酸药标签上的部分文字.某同学为了测定该药中氢氧化铝的质量分数,进行如下操作:取一片药片(药片质量0.5g),研碎后加20mL蒸馏水,然后用质量分数为5%的盐酸至反应完全(其他成分不与盐酸反应),测定实验中反应掉的盐酸为6.0g.通过计算,判断该药片中氢氧化铝的含量是否达到标准以及该药片中氢氧化铝的质量分数.查看答案和解析>>
科目: 来源: 题型:解答题
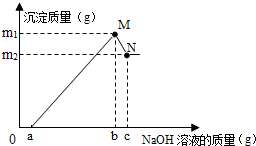 小明对废弃的易拉罐很有兴趣,他剪取W克镁铝合金的易拉罐,先用过量稀硫酸溶解,然后再向溶液中滴加一定量的NaOH溶液[已知:Al(OH)3+NaOH═NaAlO2+2H2O,Mg(OH)2不溶于NaOH溶液,假定易拉罐只由镁和铝组成],沉淀质量与滴加NaOH溶液质量关系如图所示.
小明对废弃的易拉罐很有兴趣,他剪取W克镁铝合金的易拉罐,先用过量稀硫酸溶解,然后再向溶液中滴加一定量的NaOH溶液[已知:Al(OH)3+NaOH═NaAlO2+2H2O,Mg(OH)2不溶于NaOH溶液,假定易拉罐只由镁和铝组成],沉淀质量与滴加NaOH溶液质量关系如图所示.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com