
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H+ SO42- K+ | B. | NH4+ Cl- K+ | ||
| C. | Na+ Ba2+ NO3- | D. | Cu2+ SO42- NO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 除去杂质的方法 |
| A | H2SO4 | HCl | 加入AgNO3溶液,过滤 |
| B | H2气体 | HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| C | NaCl溶液 | Na2CO3溶液 | 加入稀硫酸至不在产生气泡 |
| D | CO气体 | CO2气体 | 通过灼热的Fe2O3 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 红磷燃烧产生大量的白雾 | |
| B. | 硫在空气中燃烧,产生微弱的淡蓝色火焰 | |
| C. | 细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 木炭在氧气中剧烈燃烧,发出白光 |
查看答案和解析>>
科目: 来源: 题型:填空题
| 实验操作 | 实验现象 | 实验结论 |
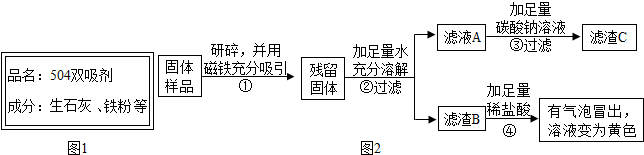
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液. | 固体溶解时试管外壁发烫,试管底部有不容物,溶液变红. | 固体中一定含有CaO 多余和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的稀HCl. | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有Fe,一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有CaCO3 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
 水是生命之源,与生产、生活关系密切.保护水环境、珍爱水资源,是每个公民应尽的责任和义务.
水是生命之源,与生产、生活关系密切.保护水环境、珍爱水资源,是每个公民应尽的责任和义务.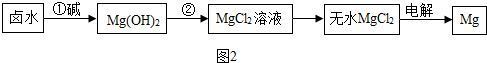
查看答案和解析>>
科目: 来源: 题型:填空题
| 元素名称 | 氟 | 氯 | 溴 | 碘 |
| 元素符号 | F | Cl | Br | I |
| 原子结构 示意图 | 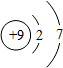 |  | 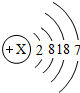 | 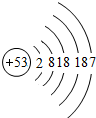 |
| 单质化学式 | F2 | Cl2 | Br2 | |
| 常温常压下 | 气态 | 液态 | 固态 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 实现CO?CO2的相互转化,都只有一种途径 | |
| B. | 铁可以实现单质$\stackrel{盐酸}{→}$氯化铁$\stackrel{NaOH}{→}$氢氧化铁 | |
| C. | 实现H2O$\stackrel{通电}{?}$O2相互转化,化学反应的基本类型不同 | |
| D. | 实现C$→_{+CuO}^{O_{2}}$CO2的转化,都利用了碳的可燃性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com