
科目: 来源: 题型:选择题
| A. | 稀释浓硫酸:为确保安全,应将水沿器壁慢慢注入浓硫酸中,并用玻璃棒不断搅拌 | |
| B. | 给试管中液体加热:试管中的液体体积不应超过试管容积的$\frac{1}{3}$ | |
| C. | 测定雨水的酸碱度:用玻璃棒蘸取待测样品滴在pH试纸上,与标准比色卡对照并、读数为5.6 | |
| D. | 粗盐提纯:在蒸发操作中,要待水分完全蒸干后再停止加热 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
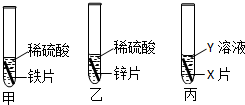
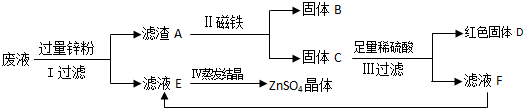
查看答案和解析>>
科目: 来源: 题型:解答题
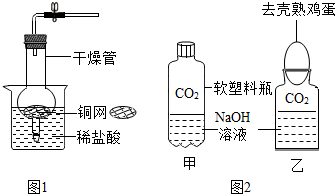 CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质:
CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质:查看答案和解析>>
科目: 来源: 题型:解答题
 根据如图所示的实验填写下列空格:
根据如图所示的实验填写下列空格:查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| 物质名称 | 固态水银 | 金 | 铜 | 铁 | 钨 | 固态氢 |
| 熔点/℃ | -38.8 | 1064 | 1083 | 1535 | 3410 | -259 |
| A. | 铜球掉入铁水中不会熔化 | B. | 在-250℃时,氢是固态的 | ||
| C. | 测量-40℃的气温应使用水银温度计 | D. | 用钨制成的灯丝不易熔化 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 样品的质量/g | 滤渣质量/g |
| 5 | 1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com