
科目: 来源: 题型:选择题
| A. | NaCl | B. | NaClO | C. | Cl2 | D. | HClO3 |
查看答案和解析>>
科目: 来源: 题型:解答题
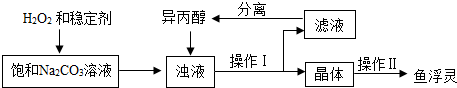
| 温度范围/℃ | 5~10 | 10~15 | 15~20 | 20~25 |
| 活性氧含量/% | 13.94 | 14.02 | 15.05 | 14.46 |
| “鱼浮灵”的产率/% | 85.49 | 85.78 | 88.38 | 83.01 |
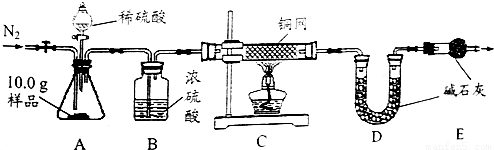
查看答案和解析>>
科目: 来源: 题型:解答题
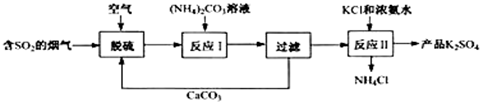
查看答案和解析>>
科目: 来源: 题型:解答题
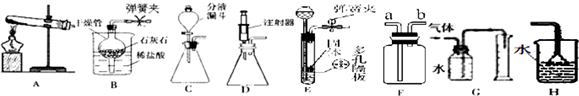
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 化学就在我们身边,它与我们的生活息息相关.
化学就在我们身边,它与我们的生活息息相关.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 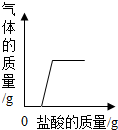 在部分变质的NaOH溶液中滴加稀盐酸 | |
| B. | 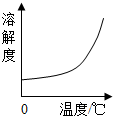 O2的溶解度受温度影响的变化曲线 | |
| C. |  等质量的Mg粉和Fe粉与足量同浓度的稀盐酸反应 | |
| D. | 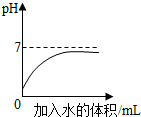 硫酸溶液稀释过程中pH的变化曲线 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 碱溶液能跟某些非金属氧化物反应,所以碱溶液能吸收CO气体 | |
| B. | 置换反应生成单质和化合物,但是有单质和化合物生成的反应不一定是置换反应 | |
| C. | 因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有碳元素、氢元素和氧元素 | |
| D. | 酸溶液能使紫色石蕊试液变红,所以能使紫色石蕊试液变红的一定是酸溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com