
科目: 来源: 题型:选择题
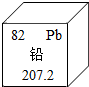 近年来,部分儿童血铅超标事件,倍受社会各界关注.铅元素相关信息如图所示.下列说法中,不正确的是( )
近年来,部分儿童血铅超标事件,倍受社会各界关注.铅元素相关信息如图所示.下列说法中,不正确的是( )| A. | 铅原子核内有82个质子 | B. | 铅有毒,儿童不能使用铅笔 | ||
| C. | 相对原子质量为207.2 | D. | 该元素属于金属元素 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | C有还原性,是该反应的还原剂 | |
| B. | 二氧化碳发生还原反应,具有还原性 | |
| C. | 镁带失火,不可以用二氧化碳灭火 | |
| D. | 该反应中所有元素均存在化合价的变化 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | N2 | B. | O3 | C. | H2 | D. | NO2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 鸡蛋放入醋中变成“软壳蛋” | B. | 用肥皂水区别硬水和软水 | ||
| C. | 用回火后的钢针作鱼钩 | D. | 用自来水清除盛石灰水瓶壁的白膜 |
查看答案和解析>>
科目: 来源: 题型:解答题
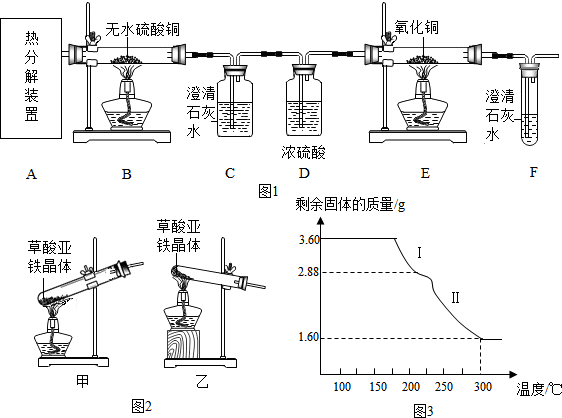
查看答案和解析>>
科目: 来源: 题型:解答题
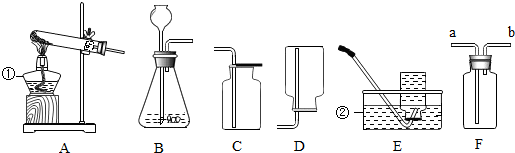
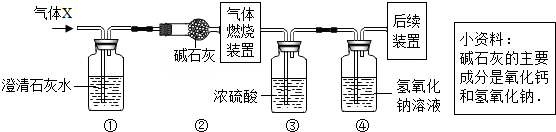
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 生活中处处有化学.
生活中处处有化学.查看答案和解析>>
科目: 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体的于试管中,加水振荡制直至完全溶解. | 不产生气泡 | 猜想Ⅰ不成立. |
| ②取少量①的溶液于试管中,滴加过量的Ba(NO3)2溶液. | 产生白色沉淀 | 证明有Na2CO3存在.化学反应方程为:Na2CO3+Ba(NO3)2═BaCO3↓+2NaNO3 |
| ③取少量②的溶液于试管中,滴加无色酚酞试液. | 酚酞试液变红 | 证明NaOH存在. |
| 结合以上实验现象,说明猜想Ⅱ是成立的. | ||
查看答案和解析>>
科目: 来源: 题型:解答题
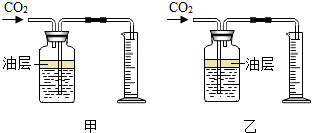 化学兴趣小组测定某石灰石样品中碳酸钙的质量分数
化学兴趣小组测定某石灰石样品中碳酸钙的质量分数查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com