
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 治疗H1N1流感病毒的良药的主要原料是莽草酸,如图为莽草酸理化性质的描述.回答下列问题:
治疗H1N1流感病毒的良药的主要原料是莽草酸,如图为莽草酸理化性质的描述.回答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题
| 实验操作 | 实验现象 | 结论 |
| ①在一杯浑浊的水中加少量硫酸钾, 用玻璃棒搅拌,静置 | 烧杯中的水 仍然浑浊 | 猜想I、Ⅱ不成立 |
| ②在一杯浑浊的水中加少量Al2(SO4)3 (写化学式),用玻璃棒搅拌,静置 | 烧杯中的水 慢慢变澄清 | 猜想Ⅲ成立 |
查看答案和解析>>
科目: 来源: 题型:解答题
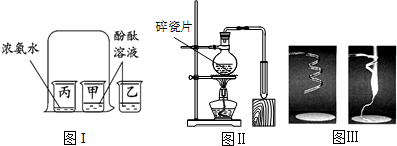
查看答案和解析>>
科目: 来源: 题型:解答题
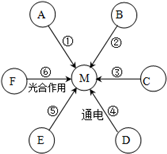 A、B、D均为纯净物,C、E、F均为混合物;①~⑥六条途径(如图)都会产生气体M,实验室可利用途径①、②、③反应来制取M,途径①、②、③、④反应类型相同,途径①反应生成的一种物质N可作为途径②、③反应的催化剂.
A、B、D均为纯净物,C、E、F均为混合物;①~⑥六条途径(如图)都会产生气体M,实验室可利用途径①、②、③反应来制取M,途径①、②、③、④反应类型相同,途径①反应生成的一种物质N可作为途径②、③反应的催化剂.查看答案和解析>>
科目: 来源: 题型:解答题
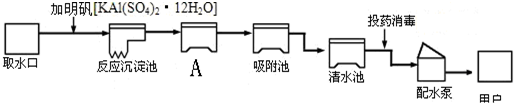
查看答案和解析>>
科目: 来源: 题型:解答题
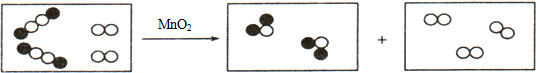
 和
和 分子个数比为2:1.
分子个数比为2:1. 质量为18g,同时生成
质量为18g,同时生成 的质量为16g,则参加反应的
的质量为16g,则参加反应的 的质量为34g.
的质量为34g.查看答案和解析>>
科目: 来源: 题型:解答题
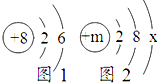 如表是元素周期表的一部分,请依据此表回答有关问题.
如表是元素周期表的一部分,请依据此表回答有关问题.| 第一 周期 | 1 H 1.008 | 2 He 4.003 | ||||||
| 第二 周期 | 3 Li 6.941 | 4 Be 9.012 | 5 B 10.81 | 6 C 12.01 | 7 N 14.01 | 8 O 16.00 | 9 F 19.00 | 10 Ne 20.18 |
| 第三 周期 | 11Na 22.99 | 12Mg 24.31 | 13 Al 26.98 | 14 Si 28.09 | 15 P 30.97 | 16 S 32.06 | 17 Cl 35.45 | 18 Ar 39.95 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com