
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
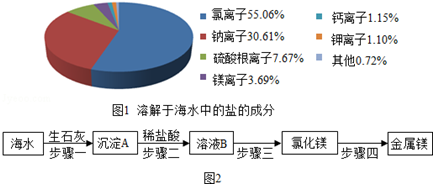
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
| 物质 | 乙 醇 | 氧 气 | 二氧化碳 | 水蒸气 | w |
| 反应前质量/g | 23 | 40 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 22 | 27 | x |
查看答案和解析>>
科目: 来源: 题型:选择题
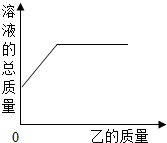 在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量的关系,能用如图曲线表示的是( )
在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量的关系,能用如图曲线表示的是( ) | 序号 | 甲 | 乙 |
| ① | HCl溶液 | NaOH溶液 |
| ② | HCl溶液 | 大理石 |
| ③ | CaCl2溶液 | Na2CO3溶液 |
| ④ | CuSO4溶液 | 铁粉 |
| ⑤ | H2SO4溶液 | 锌粒 |
| A. | ①② | B. | ③④ | C. | ①⑤ | D. | ②⑤ |
查看答案和解析>>
科目: 来源: 题型:解答题
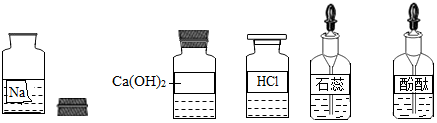
查看答案和解析>>
科目: 来源: 题型:解答题
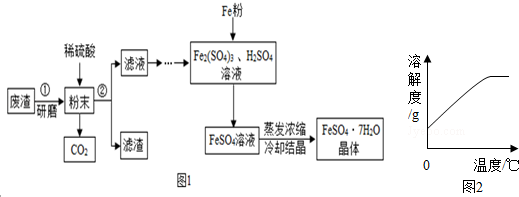
查看答案和解析>>
科目: 来源: 题型:解答题
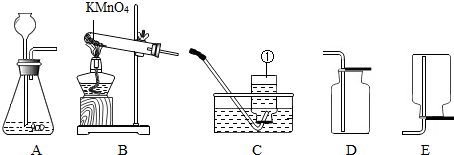
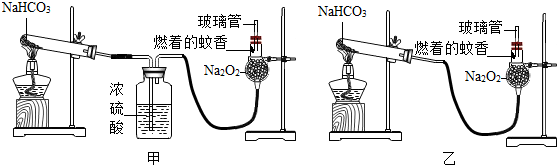
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com