
科目: 来源: 题型:解答题

| 物质 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
| 开始沉淀时pH | 6.34 | 1.48 | 6.2 | 5.2 |
| 完全沉淀时pH | 9.7 | 3.2 | 8.0 | 6.4 |
| Fe(OH)2是一种絮状沉淀,不易除去,处理时常将其转化为Fe(OH)3而除去. | ||||
查看答案和解析>>
科目: 来源: 题型:解答题
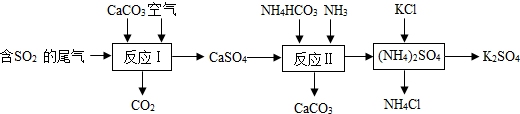
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 若a=1,则b=2 | |
| B. | a+b可能大于4 | |
| C. | 反应后金属的质量不可能超过21.6g | |
| D. | 当得到的金属质量为20 g时,a一定等于3 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
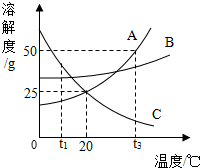 A、B、C三种物质的溶解度曲线如图所示.
A、B、C三种物质的溶解度曲线如图所示.查看答案和解析>>
科目: 来源: 题型:解答题
| 项目 | 标准 |
| 感官指标 | 无异味、异臭等 |
| 化学指标 | pH6.5-8.5,铜<1.0mg•L-1,氟化物<1.0mg•L-1,游离氯≥0.3mg•L-1等 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | pH越小,溶液的酸性越弱 | |
| B. | pH小于7的雨水是酸雨 | |
| C. | 胃酸过多的病人在空腹时不宜多喝柠檬汁 | |
| D. | 用广范试纸测出某溶液的pH=3.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com