
科目: 来源: 题型:选择题
| A. | 老酒的主要成分是酒精和水,有一定的颜色,是乳浊液 | |
| B. | 老酒选用优质糯米发酵而成,发酵要利用酵母菌的无氧呼吸,是有性生殖 | |
| C. | 老酒在贮存过程中,乙醇等物质挥发,酒精度下降,是利用了乙醇的化学性质 | |
| D. | 老酒越陈越醇,在老酒的陈化过程中,生成了一种有香味的酯,是化学变化 |
查看答案和解析>>
科目: 来源: 题型:解答题
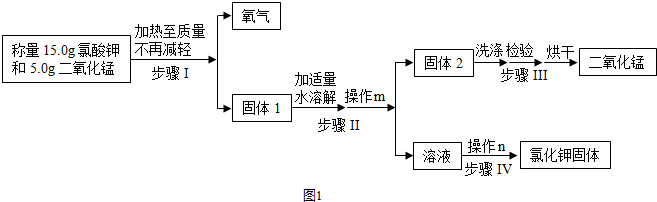

查看答案和解析>>
科目: 来源: 题型:选择题
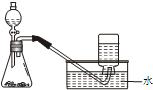 下列制取气体的方案,可以直接采用如图所示装置进行的是( )
下列制取气体的方案,可以直接采用如图所示装置进行的是( )| A. | 只有① | B. | ①④ | C. | ①②③④ | D. | ②③ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
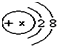 ,若X等于11,则该微粒表示阳(填“阳”或“阴”)离子.
,若X等于11,则该微粒表示阳(填“阳”或“阴”)离子.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
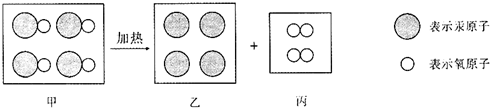
| A. | 图中甲、乙、丙三种物质均是由分子构成的 | |
| B. | 图中甲、乙、丙三种物质均含有氧元素 | |
| C. | 图中甲、乙、丙三种物质既有单质又有化合物 | |
| D. | 该反应前后分子种类、原子种类均没有改变 |
查看答案和解析>>
科目: 来源: 题型:选择题
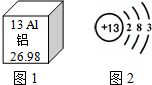
| A. | 铝元素原子核内的中子数为13 | |
| B. | 铝的相对原子质量为26.98 g | |
| C. | 铝离子的核外电子分三层排布 | |
| D. | 铝元素的化学性质与铝原子的最外层电子数有密切的关系 |
查看答案和解析>>
科目: 来源: 题型:解答题
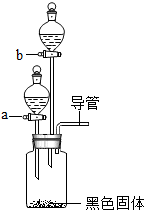 不少家庭养观赏鱼,有时会在鱼缸里放点“鱼浮灵”,可使水中的含氧量迅速增加.请你和小欣同学一起完成这项探究活动.
不少家庭养观赏鱼,有时会在鱼缸里放点“鱼浮灵”,可使水中的含氧量迅速增加.请你和小欣同学一起完成这项探究活动.| 实验 | 主要操作步骤 | 主要实验现象 | 结论 |
| ① | 在集气瓶中加入少量二氧化锰(黑色固体),在仪器a中加入新配制的“鱼浮灵”的饱和水溶液;打开仪器a的活塞,放出适量溶液后,在导管口放一根带火星的木条 | 有气泡逸出,能使带火星木条复燃 | “鱼浮灵”溶于水生成过氧化氢 |
| ② | 关闭仪器a,在仪器b中加入稀盐酸,打开活塞,放出适量溶液后,在导管口放一燃着的木条 | 生成大量无色气泡,木条熄灭 | “鱼浮灵”溶于水生成碳酸钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com