
科目: 来源: 题型:选择题
| A. | 煤炭直接燃烧 | B. | 秸秆焚烧还田 | ||
| C. | 开发清洁能源 | D. | 通过加高烟囱排放工业废气 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 由方法一,二反应原理可知:氧化还原反应的特征是有单质生成 | |
| B. | 方法二优于方法一的主要原因是制备过程中不产生氯气 | |
| C. | 方法一中氯元素有五种化合价 | |
| D. | 氯气是由氯离子构成的 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 实验室中浓硫酸的标签如图所示.请根据有关信息计算:
实验室中浓硫酸的标签如图所示.请根据有关信息计算:查看答案和解析>>
科目: 来源: 题型:解答题
| 实验事实(至少举两例) | 实验结论 | 结论的应用(举例说明) |
| 示例:铁、铝等活泼金属能和酸发生反应生成氢气 | 活泼金属能和酸发生反应生成氢气 | 锌也能和酸反应生成氢气 |
| 氢氧化钠、氢氧化钙溶液都能使无色酚酞变红 | 碱溶液能使无色酚酞变红 | |
查看答案和解析>>
科目: 来源: 题型:解答题
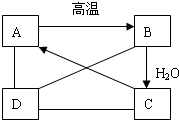 有A、B、C、D四种物质,如图所示,A、B、C在一定下可以发生转化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,D与C发生中和反应,D与A反应有CO2气体产生.
有A、B、C、D四种物质,如图所示,A、B、C在一定下可以发生转化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,D与C发生中和反应,D与A反应有CO2气体产生.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com