
科目: 来源: 题型:选择题
| A. | 元素和原子都是构成物质的基本微粒 | |
| B. | 元素是宏观的抽象概念,无数量意义 | |
| C. | 原子是微观的具体实物,有数量意义 | |
| D. | 元素是核电荷数相同的一类原子的总称 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 所有原子的原子核都是由质子和中子构成的 | |
| B. | 相对原子质量表示原子的相对质量 | |
| C. | 同种物质的分子性质相同,不同种物质的分子性质不同 | |
| D. | 分子是构成物质的唯一微粒 |
查看答案和解析>>
科目: 来源: 题型:解答题
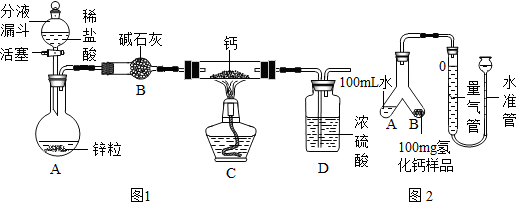
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题


查看答案和解析>>
科目: 来源: 题型:解答题
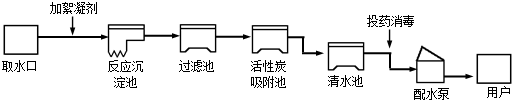
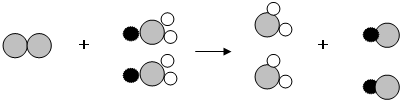
 表示氯原子,
表示氯原子, 表示钠原子,
表示钠原子, 表示氧原子)
表示氧原子)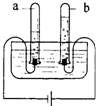
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com