
科目: 来源: 题型:填空题
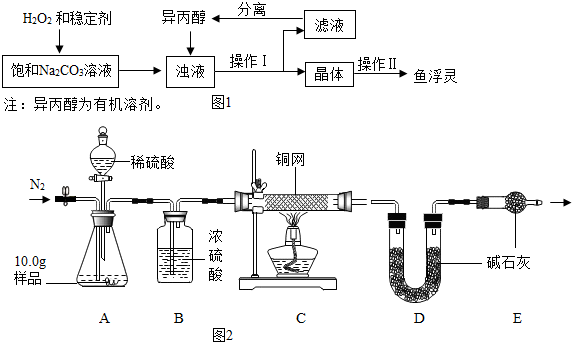
| 温度范围/℃ | 5~10 | 10~15 | 15~20 | 20~25 |
| 活性氧含量/% | 13.94 | 14.02 | 15.05 | 14.46 |
| “鱼浮灵”的产率/% | 85.49 | 85.78 | 88.38 | 83.01 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
 实验室有半瓶敞口放置的标签残缺的白色固体(标签如图),小明、小亮根据初中所学的知识进行下列探究.
实验室有半瓶敞口放置的标签残缺的白色固体(标签如图),小明、小亮根据初中所学的知识进行下列探究.| 实验步骤 | 实验现象 | 结论 |
| A.取少量滤液加入过量的BaCl2溶液 | 产生白色沉淀 | 一定有Na2CO3 |
| B.将A中的混合物过滤,向滤液中加酚酞试液 | 溶液变成红色 | 一定有NaOH |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 铜粉(炭粉)--在空气中灼烧 | |
| B. | 硫酸钾溶液(碳酸钾)--适量的稀硫酸 | |
| C. | 氧气(氢气)--点燃 | |
| D. | 氯化亚铁溶液(氯化铁)一一氢氧化钠溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 扎那米韦属于有机高分子化合物 | |
| B. | 扎那米韦的相对分子质量为332 | |
| C. | 1个扎那米韦分子由12个碳原子、20个氢原子、4个氮原子和7个氧原子构成 | |
| D. | 扎那米韦中碳元素、氢元素和氮元素的质量比为3:5:1 |
查看答案和解析>>
科目: 来源: 题型:填空题
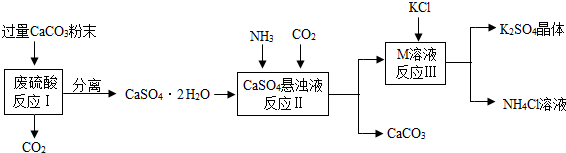
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
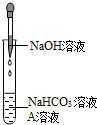 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 现象Ⅰ | 无明显变化 | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com