
科目: 来源: 题型:选择题
| A. | 用塑化剂制奶茶 | B. | 使用地沟油做火锅 | ||
| C. | 甲醛水溶液泡制水产品 | D. | 用小苏打做发酵粉制作面点 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na+ K+ SO42- | B. | H+ Cu2+ SO42- | ||
| C. | Na+ NH4+ NO3- | D. | Cu2+ NO3- CO32- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$ CO2+2H2O | B. | CO2+Ca(OH)2═CaCO3↓+H2O | ||
| C. | CaCO3+2HCl═CaCl2+CO2↑+H2O | D. | 3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 铝制品比铁制品耐腐蚀,说明铁比铝的金属活动性强 | |
| B. | 过氧化氢溶液中加入二氧化锰,立即产生气体,证明二氧化锰是该反应催化剂 | |
| C. | 纯碱的水溶液呈碱性,说明纯碱中含有烧碱 | |
| D. | 碳燃烧可生成CO或CO2,说明反应物的质量关系不同,产物可能不同 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用过滤的方法除去粗盐中的可溶性杂质 | |
| B. | 用燃烧木炭的方法可制得纯净的二氧化碳气体 | |
| C. | 用浓硫酸除去氢气中的水蒸气 | |
| D. | 用无色酚酞溶液鉴别稀盐酸和食盐水 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 石油和钢都是混合物 | B. | 水银和液态氧都是单质 | ||
| C. | 冰水混合物和干冰都是化合物 | D. | 蒸馏水和矿泉水都是纯净物 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
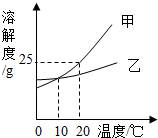 如图表示的是甲、乙两种固体物质的溶解度曲线,请回答:
如图表示的是甲、乙两种固体物质的溶解度曲线,请回答:查看答案和解析>>
科目: 来源: 题型:解答题
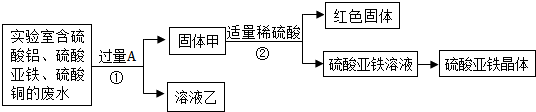
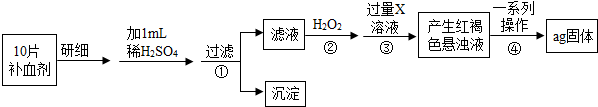
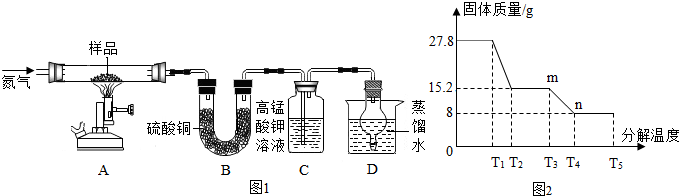
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com