
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
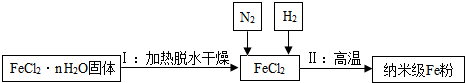
| A. | 将FeCl2﹒nH2O加热脱水干燥的原因可能是生成的纳米级铁粉会与水反应 | |
| B. | Ⅱ中反应的化学方程式为 H2+FeCl2$\frac{\underline{\;高温\;}}{\;}$Fe+2HCl | |
| C. | 纳米级Fe粉比普通 Fe粉更易与氧气反应 | |
| D. | N2未参加反应,因此在实验中可以不通N2 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验操作 | 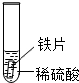 | 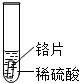 | 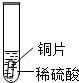 |
| 实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变为蓝色 | 无明显现象发生(或无气泡生成,溶液也不变色) |
查看答案和解析>>
科目: 来源: 题型:解答题
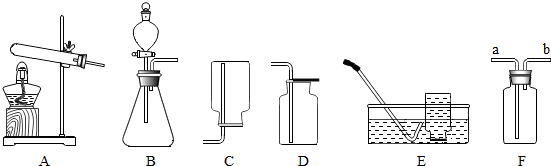
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①属于化合反应 | B. | ②属于置换反应 | C. | ③属于复分解反应 | D. | ④属于置换反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
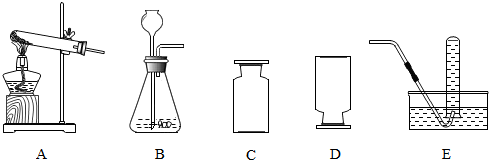
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com