
科目: 来源: 题型:选择题
| A除去CO中的CO2 | B 探究二氧化锰对反应速率的影响 | C 探究空气中氧气含量 | D探究溶解性的影响因素 |
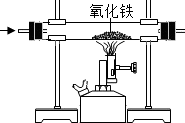 | 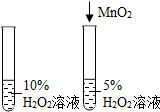 | 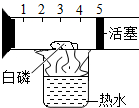 | 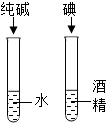 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
| FeCl2溶液 | FeCl3溶液 | |
| 加入Fe粉 | 无明显变化 | 溶液变成浅绿色 |
| 加KSCN溶液 | 无明显变化 | 溶液变成红色 |
| 实验操作 | 实验现象 | 结论与解释 |
| ①取少量的黑色固体于试管中,滴加适量的稀盐酸 ②向步骤①所得的溶液中,滴加KSCN溶液 | 甲组: 固体溶解,无气泡冒出 加KSCN溶液后,溶液变成红色 | 甲组用CO还原Fe2O3反应的化学方程式是CO+3Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe3O4+CO2 |
| 乙组: 固体溶解,有气泡冒出 加KSCN溶液后,溶液颜色无明显变化 | 黑色固体的成分是Fe |
查看答案和解析>>
科目: 来源: 题型:解答题
 某化学兴趣小组的同学用如图所示装置进行以下三个实验.
某化学兴趣小组的同学用如图所示装置进行以下三个实验.查看答案和解析>>
科目: 来源: 题型:解答题
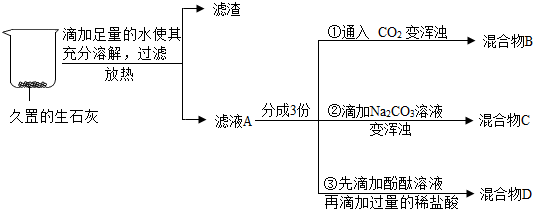
查看答案和解析>>
科目: 来源: 题型:解答题
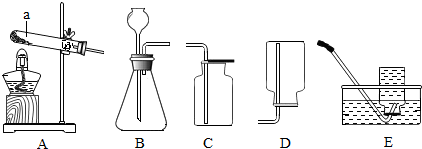
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com