
科目: 来源: 题型:选择题
| A. | 茶氨酸由碳、氢、氧、氮四种原子构成 | |
| B. | 茶氨酸属于有机物,锌、硒指单质 | |
| C. | 茶氨酸中碳、氢、氧、氮四种元素的质量比是7:14:3:2 | |
| D. | 茶氨酸的化学式量是174 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 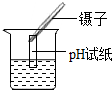 测溶液pH | B. | 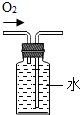 排水法收集氧气 | C. | 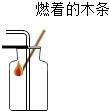 CO2气体验满 | D. |  给液体加热 |
查看答案和解析>>
科目: 来源: 题型:解答题
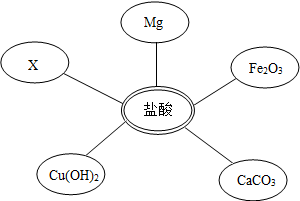
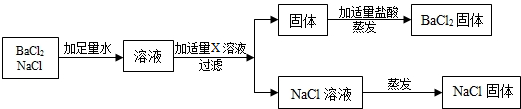
| 方案 | 加入试剂 | 提纯的方法 | 方案评价 |
| 一 | 适量Ca(NO3)2溶液 | 过滤、蒸发结晶 | (选填可行或不可行) |
| 二 | 稍过量的盐酸(或稀HCl或HCl) | 蒸发结晶 | 可行 |
查看答案和解析>>
科目: 来源: 题型:解答题
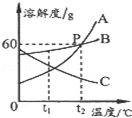 如图为A、B、C三种固体物质的溶解度曲线,根据图示完成问题:
如图为A、B、C三种固体物质的溶解度曲线,根据图示完成问题:查看答案和解析>>
科目: 来源: 题型:解答题
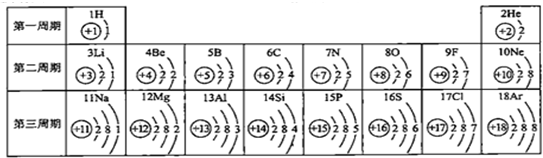
查看答案和解析>>
科目: 来源: 题型:解答题
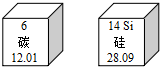 图中是两种元素在周期表中的信息.请回答下列问题
图中是两种元素在周期表中的信息.请回答下列问题查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com