
科目: 来源: 题型:选择题
| A. | CO和CO2分子构成不同,则化学性质不同 | |
| B. | 同一化合物中,金属元素显正价,则非金属元素一定显负价 | |
| C. | 氢氧化铝可治疗胃酸过多,则氢氧化钠也可治疗胃酸过多 | |
| D. | 烧碱属于碱,则纯碱也属于碱 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 该图表示的是一个化合反应 | |
| B. | 该反应中一定有元素的化合价变化 | |
| C. | 该反应中,原子发生重新组合 | |
| D. | 该反应中,反应物、生成物的微粒个数比为2:2:2:1 |
查看答案和解析>>
科目: 来源: 题型:解答题
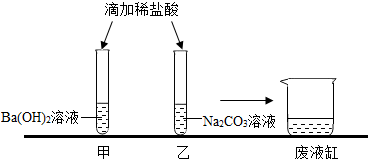
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将氢氧化钠固体直接放在托盘天平的托盘上称量 | |
| B. | 点燃一氧化碳前,应先检查气体的纯度 | |
| C. | 为节约药品,实验室用剩的药品应放回原瓶 | |
| D. | 用量筒量取一定量的液体时,仰视刻度 |
查看答案和解析>>
科目: 来源: 题型:解答题
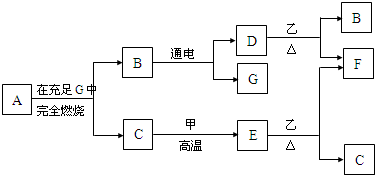
查看答案和解析>>
科目: 来源: 题型:解答题
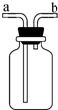 可燃冰也称为“甲烷水合物”.“置换法”是开采可燃冰设想方案之一,即将CO2注入海底的甲烷水合物储层,将甲烷水合物中的甲烷分子“挤走”,从而将其“置换”出来:(原理:CH4•nH2O+CO2═CO2•nH2O+CH4).
可燃冰也称为“甲烷水合物”.“置换法”是开采可燃冰设想方案之一,即将CO2注入海底的甲烷水合物储层,将甲烷水合物中的甲烷分子“挤走”,从而将其“置换”出来:(原理:CH4•nH2O+CO2═CO2•nH2O+CH4).查看答案和解析>>
科目: 来源: 题型:解答题

| 小组 | 取用石灰石样品质量 | 测得CO2的质量 | 碳酸钙的质量分数 |
| ① | 1.0g | 0.90g | 204% |
| ② | 2.0g | 0.80g | 91% |
| ③ | 2.5g | 1.0g | 93% |
| ④ | 3.0g | 1.2g | 92% |
查看答案和解析>>
科目: 来源: 题型:解答题
| 甲 | 乙 | 丙 | |
| 所取样品质量 | 25g | 30g | 25g |
| 加入的盐酸质量 | 100g | 100g | 150g |
| 充分反应后溶液质量 | 116.2g | 121.2g | 166.2g |
查看答案和解析>>
科目: 来源: 题型:解答题
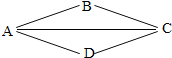 金属和酸、碱、盐的化学性质是初中化学的核心知识,如图,A、B、C、D分别表示上述四类物质中常见的一种,A、B、C、D之间的连线表示它们彼此之间能够发生化学反应,其中A与B能够发生中和反应,D是目前世界上产量最多的金属.
金属和酸、碱、盐的化学性质是初中化学的核心知识,如图,A、B、C、D分别表示上述四类物质中常见的一种,A、B、C、D之间的连线表示它们彼此之间能够发生化学反应,其中A与B能够发生中和反应,D是目前世界上产量最多的金属.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com