
科目: 来源: 题型:选择题
| A. | Fe2+、H+、Cl- | B. | H+、Cl-、CO32- | C. | K+、Cu2+、OH- | D. | H+、OH-、Na+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该物质的每个分子中含有22个原子 | |
| B. | 该物质分子中,碳、氢、氧原子个数比为5:12:5 | |
| C. | 该物质中,碳、氢、氧三种元素的质量比为5:12:5 | |
| D. | 该物质的相对分子质量为152 |
查看答案和解析>>
科目: 来源: 题型:解答题
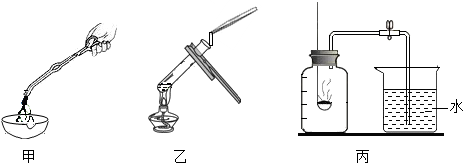
| 反应前镁带的质量/g | 反应后的固体产物的质量/g |
| 2.4024 | 3.8839 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验 | 1 | 2 | 3 | 4 |
| 加入盐酸的质量/g | 50 | 100 | 150 | 200 |
| 生成CO2的质量/g | 1.76 | 3.52 | 4.4 | m |
查看答案和解析>>
科目: 来源: 题型:解答题
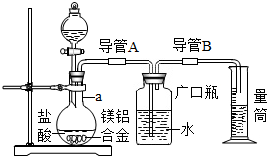 含镁3%~5%的镁铝合金是轮船制造、化工生产、机械制造等行业的重要原材料.现有一块质量为wg的镁铝合金,某研究性学习小组欲测定其中镁的质量分数.
含镁3%~5%的镁铝合金是轮船制造、化工生产、机械制造等行业的重要原材料.现有一块质量为wg的镁铝合金,某研究性学习小组欲测定其中镁的质量分数.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 可以用铁桶盛放浓硫酸,但在清洗盛放过浓硫酸的铁桶时,不能遇明火 | |
| B. | 茶壶里的水垢,可以用醋酸或纯碱溶液除去 | |
| C. | 用天平称取NaOH固体时,必须将NaOH固体放在称量纸上 | |
| D. | 除去硫酸铁溶液中混有的硫酸,可以往其中加入铁粉 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②③④ | B. | ①③④ | C. | ②③④ | D. | ②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com