
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
 框图中“→”表示物质之间可以向箭头所指方向一步转化.若A、B、C、D是常见的金属Fe、Al、Mg、Cu四种中的一种,则A、B、C、D依次是( )
框图中“→”表示物质之间可以向箭头所指方向一步转化.若A、B、C、D是常见的金属Fe、Al、Mg、Cu四种中的一种,则A、B、C、D依次是( )| A. | Fe、Al、Mg、Cu | B. | Mg、Al、Cu、Fe | C. | Mg、Al、Fe、Cu | D. | Al、Mg、Fe、Cu |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 盐酸能与锌粒反应生成气体 | |
| B. | 稀硫酸能与氯化钡溶液反应生成白色沉淀 | |
| C. | 醋酸能除水垢(主要成分是碳酸钙) | |
| D. | 稀盐酸能除铁锈 |
查看答案和解析>>
科目: 来源: 题型:选择题
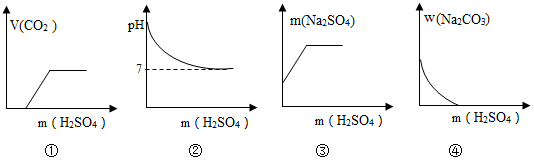
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 甲醛是一种酸 | |
| B. | 甲醛是由氢元素、氧元素和碳元素组成的一种氧化物 | |
| C. | 甲醛有挥发性 | |
| D. | 甲醛分子中碳、氢、氧各原子的个数比为1:1:2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 测溶液pH时将洁净的玻璃棒蘸取被测溶液滴到湿润的pH试纸上 | |
| B. | 稀释浓硫酸时,可将浓硫酸慢慢倒入盛有水的量筒中并搅拌 | |
| C. | 点燃氢气前,要先检验氢气的纯度 | |
| D. | 用托盘天平可以准确称量10.58gNa2CO3粉末 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com