
科目: 来源: 题型:解答题
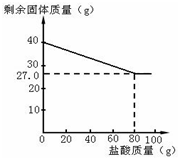 某化学兴趣小组的同学为测定假黄金(铜锌合金)中各组成元素的质量分数,称取40克假黄金置于烧杯中,用某浓度的稀盐酸100克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下:
某化学兴趣小组的同学为测定假黄金(铜锌合金)中各组成元素的质量分数,称取40克假黄金置于烧杯中,用某浓度的稀盐酸100克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下:| 实验次数 | 稀盐酸的用量(g) | 剩余固体的质量(g) |
| 1 | 20 | 36.75 |
| 2 | 20 | 33.50 |
| 3 | 20 | 30.25 |
| 4 | 20 | 27.00 |
| 5 | 20 | 27.00 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 草酸(H2C2O4)是一种固体,常用于制CO,受热时发生如下反应:
草酸(H2C2O4)是一种固体,常用于制CO,受热时发生如下反应:查看答案和解析>>
科目: 来源: 题型:解答题
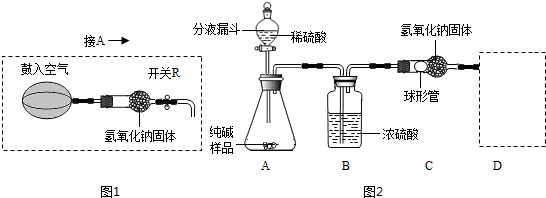
查看答案和解析>>
科目: 来源: 题型:解答题
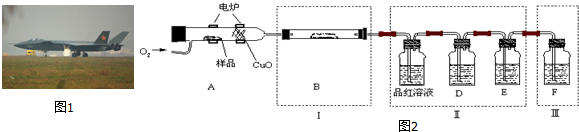
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
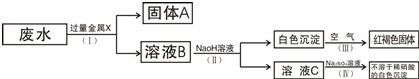
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CaCl2 | HCl | 加入过量 CaCO3,过滤 |
| B | H2SO4 | HNO3 | 加入适量Ba(NO3)2溶液,过滤 |
| C | NaCl | Na2CO3 | 加人适量的Ca(OH)2溶液、过滤 |
| D | Na2SO4溶液 | CuSO4 | 加入过量氢氧化钠溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com