18.氢化钙(CaH
2)是一种常用的储氢材料,也是登山运动员常用的能源提供剂.
【资料】
Ⅰ.金属钙的活动性很强,遇水即刻剧烈反应生成氢氧化钙,同时产生氢气.
Ⅱ.氢化钙要密封保存,一旦接触到水就发生反应,放出氢气.
探究一:氢化钙与水反应的生成物
猜想一:氧化钙和氢气;猜想二:氢氧化钙和氢气.
(1)你认为猜想一错误,你的理由是根据水中氢原子和氧原子的个数比不符.
(2)CaH
2中氢元素的化合价是-1,写出CaH
2与水反应的化学方程式CaH
2+2H
2O=Ca(OH)
2+2H
2↑.
探究二:实验室制备氢化钙
用氢气与金属钙加热可得到氢化钙,实验装置和步骤如图所示:
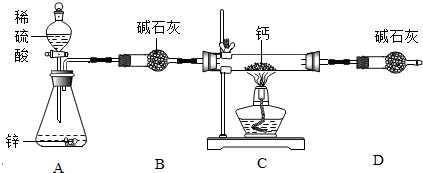
①检查装置气密性;②装入药品并打开分液漏斗;③加热反应一段时间;④停止加热,充分冷却;⑤关闭分液漏斗活塞.
(1)步骤①中检查气密性的方法是:关闭分液漏斗的活塞,先把导管的一端放入水中,然后两手紧握锥形瓶的外壁,观察导管口是否有气泡冒出.
(2)装置B的作用是吸水干燥作用;若要证明进入装置C的氢气已经干燥,应在BC之间(填装置序号)增加装有无水硫酸铜(试剂名称)的U型管.
(3)实验时先打开装置A中的活塞,一段时间后,再点燃装置C中的酒精灯,其目的是排出空气,避免爆炸.
(4)上述实验步骤存在安全隐患,有同学建议应先预热再进行加热.
(5)制备CaH
2实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,在溶液中滴入酚酞后显红色.该同学据此判断:上述实验中确有CaH
2生成.请你判断他的结论是否正确并说明理由不正确,因为氢化钙与水反应生成氢氧化钙和氢气,钙与水剧烈反应也生成氢氧化钙,同时产生氢气;都生成氢氧化钙,氢氧化钙显碱性,因此滴入酚酞后显红色.
(6)经讨论,小组同学认为,可以通过固体质量的变化判断反应的发生.若反应前固体的质量为a,反应后固体的质量为b,a<b(填“>”“<”“=”),则说明反应发生.
探究三:产品含量测定
通过上述方法制得的氢化钙样品是否纯净?某兴趣小组的同学设计了几组实验进行验证.
甲组样品纯度的测定装置如图所示:A为发生装置,B为储液瓶,C为液体量瓶(有刻度).
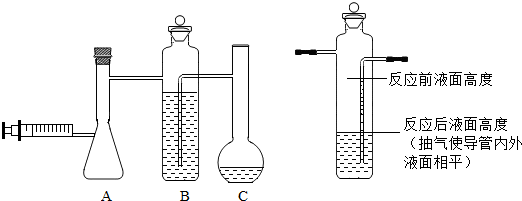
(1)实验前C中液体为120ml,实验时将注射器中100ml的水缓缓推入A装置,完全反应后,B中状况如图所示,再用注射器抽气使B中导管内外液面相平,最终C中液体为860ml,注射器中活塞停留在10mL处.则生成氢气0.75L.
(2)上述操作中抽气的原因是将生成的氢气全部吸入锥形瓶中.
乙组同学也采用测量氢气体积的方法来测定氢化钙的纯度.装置及步骤如图所示:
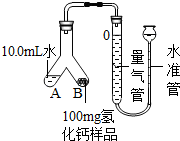
①检查装置气密性,装入药品;②调整水准管高度,使量气装置两边的液面保持同一水平.读取液面所在的刻度数据为10.0mL;③将Y形管慢慢倾斜,直到A端的水全部与B端的样品混合.④反应结束,冷却至室温,调节两端液面齐平,再次读取液面所在刻度数据为110.0mL.
(3)如何判断样品与水完全反应:量气管中液面不再变化.
(4)读取量气管读数时,除了调节量气管和水准管的液面相平,还需视线与凹液面最低处相平.
(5)已知该条件下,氢气的密度为0.09mg/cm
3.样品中氢化钙的纯度为88.4%.(精确到0.1%)
丙组同学取乙组完全反应后的Y形管继续实验.
(6)观察管内有较多白色不溶物,请分析不溶物的成分为Ca(OH)
2(填写化学式),其不溶的原因的是氢化钙和水反应放出大量的热,氢氧化钙在水中的溶解度随温度的升高而减小,且氢氧化钠在水中的溶解度较小.
丙组同学向Y型管中滴加稀盐酸至pH=4,蒸干反应后的液体称量所得固体的质量,由此计算氢化钙的纯度.
滴加盐酸至pH=4的目的是将氢氧化钙全部转化成氯化钙.
(7)该组某同学提出只要称量Y形管反应前后的质量差,也能计算氢化钙的纯度.你认为该方法是否准确并说明理由:不准确,氢化钙和水反应放出大量的热,一定量的水蒸气会进入量气管,是Y型管内的质量差偏大.

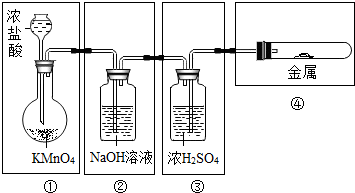 已知KMnO4与浓HCl在常温下反应能产生氯气(Cl2),Cl2黄绿色、易溶于水、有毒性,能被氢氧化钠溶液吸收.若用图示的实验装置来制备纯净、干燥的氯气,并试验它在常温下与金属的反应,每个虚线框表示一个单元装置,其中存在明显错误的是( )
已知KMnO4与浓HCl在常温下反应能产生氯气(Cl2),Cl2黄绿色、易溶于水、有毒性,能被氢氧化钠溶液吸收.若用图示的实验装置来制备纯净、干燥的氯气,并试验它在常温下与金属的反应,每个虚线框表示一个单元装置,其中存在明显错误的是( )


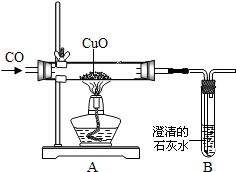 一氧化碳是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如下实验装置.请回答以下有关问题:
一氧化碳是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如下实验装置.请回答以下有关问题: