
科目: 来源: 题型:选择题
| A. | 0.12% | B. | 0.24% | C. | 1.2×10-4% | D. | 2.4×10-4% |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2SO4和Na2SO3 | B. | Na2CO3和NaHCO3 | C. | KNO2和KMnO4 | D. | AgNO3和NH4NO3 |
查看答案和解析>>
科目: 来源: 题型:解答题
 某实验小组利用如图装置测量空气中氧气体积分数并取得成功.
某实验小组利用如图装置测量空气中氧气体积分数并取得成功.查看答案和解析>>
科目: 来源: 题型:解答题
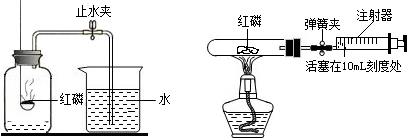
查看答案和解析>>
科目: 来源: 题型:解答题
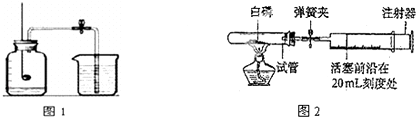
查看答案和解析>>
科目: 来源: 题型:解答题
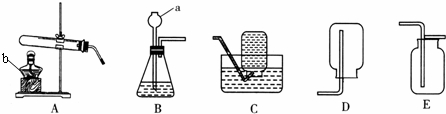
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 测量空气中氧气的含量时,点燃红磷后要迅速伸入集气瓶中 | |
| B. | 把双氧水从分液漏斗迅速加入装有少量二氧化锰粉末的锥形瓶中 | |
| C. | 把点燃的木炭放入燃烧匙内,由上而下缓慢伸入集满氧气的集气瓶中 | |
| D. | 在试管中加入几小块大理石,先平放在试管口,再缓慢竖直试管 |
查看答案和解析>>
科目: 来源: 题型:解答题
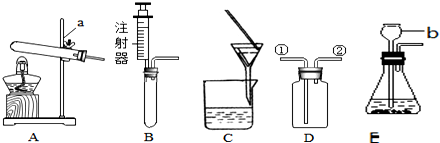
查看答案和解析>>
科目: 来源: 题型:解答题
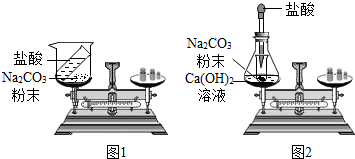 某班同学按如图所示的实验探究质量守恒定律.
某班同学按如图所示的实验探究质量守恒定律.| A | B | C | D | |
| 盐酸加入Na2 CO3粉末前称量/g | 85.3 | 82.8 | 84.8 | 86.5 |
| 盐酸加入Na2 CO3粉末后称量/g | 85.3 | 80.6 | 83.2 | 87.8 |
查看答案和解析>>
科目: 来源: 题型:解答题
 如图实验装置.请回答以下有关问题:
如图实验装置.请回答以下有关问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com