
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 钢铁、铝合金、铜制品等是应用广泛的金属材料.据估计,每年全世界被腐蚀损耗的钢铁材料,约占全年钢产量的十分之一.某校化学兴趣小组的同学探究金属腐蚀的原因,设计如下实验:
钢铁、铝合金、铜制品等是应用广泛的金属材料.据估计,每年全世界被腐蚀损耗的钢铁材料,约占全年钢产量的十分之一.某校化学兴趣小组的同学探究金属腐蚀的原因,设计如下实验:| 实验操作 | 实验现象 | 结论 | |
步骤l | 取少量石青样品置于大试管中加入足量稀硫酸 | (1)产生大量气体 (2)溶液呈蓝色 | (1)石青中含有CO32-离子 (2)石青中含有Cu2+离子 |
步骤2 | 取少量石青样品置于大试管中加热 | (1)残留固体呈黑色 (2)大试管内壁有水珠 | 石青加热易分解 |
查看答案和解析>>
科目: 来源: 题型:选择题
| X盐溶液 | Y盐溶液 | Z盐溶液 | |
| Ni | 无 | 无 | 有 |
| Mn | 无 | 有 | 有 |
| A. | X Mn Y Ni Z | B. | Z Ni Y Mn X | ||
| C. | Z Mn Y Ni X | D. | X Mn Ni Y Z |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
| 操作 |  |  | 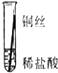 | 根据现象得出金属活动性顺序 |
| 片刻后现象 | 有少量气泡 | 无气泡 | 无气泡 | Fe>Al,Fe>Cu |
| 几分钟后现象 | 有少量气泡 | 有大量气泡 | 无气泡 |
| 操作 | 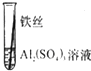 | 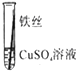 | 根据现象得出金属活动性顺序 |
| 现象 | 无明显现象 | Al>Fe>Cu |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Fe+HCl Cu+HCl Fe+Hg(NO3)2 | B. | Fe+HCl Fe+Hg(NO3)2 Cu+Hg(NO3)2 | ||
| C. | Fe+HCl Cu+HCl Cu+Hg(NO3)2 | D. | Cu+HCl Fe+Hg(NO3)2 Cu+Hg(NO3)2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 黄铜和铜相比,强度和硬度都要高一些 | |
| B. | 一般在水龙头表面镀铬以防生锈 | |
| C. | 银的导电性比铜好,应该提倡使用银制导线 | |
| D. | 钛合金与人体具有很好的相容性,可用来制造人造骨 |
查看答案和解析>>
科目: 来源: 题型:解答题
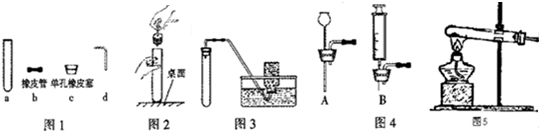
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com