
科目: 来源: 题型:选择题
| A. | Cl-、NO3-、Ag+、Na+ | B. | Na+、Cl-、OH-、Fe3+ | ||
| C. | SO42-、NO3-、K+、H+ | D. | Ca2+、Cl-、CO32-、K+ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
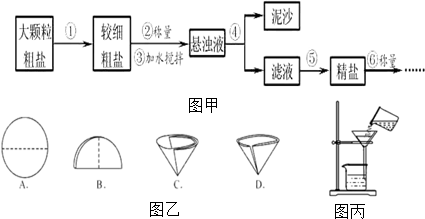
查看答案和解析>>
科目: 来源: 题型:解答题
| 因素 | 第一组 | 第二组 | 第三组 | ||
| 实验温度 | 20℃ | 20℃ | 20℃ | 20℃ | 80℃ |
| 加入溶剂种类 | 水 | 酒精 | 水 | 水 | 水 |
| 加入溶剂质量 | 20g | 20g | 10g | 10g | 10g |
| 加入固体种类 | 硝酸钾 | 硝酸钾 | 硝酸钾 | 食盐 | 硝酸钾 |
| 加入固体质量 | 10g | 10g | 10g | 10g | 10g |
| 溶解固体质量 | 6.2g | 0g | 3.1g | 3.6g | 10g |
查看答案和解析>>
科目: 来源: 题型:解答题
 如图是甲、乙两种固体溶解度曲线回答下列问题:
如图是甲、乙两种固体溶解度曲线回答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题
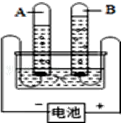 如图所示是一种电解水的装置,请回答下列问题
如图所示是一种电解水的装置,请回答下列问题查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 收集雨水作为生活用水 | B. | 用淘米水浇花 | ||
| C. | 推广使用节水龙头 | D. | 工业污水不经处理直接排放 |
查看答案和解析>>
科目: 来源: 题型:解答题
 定性和定量结合既是化学的重要思想,也是研究物质组成的重要方法.某研究性学习小组为检测实验室用H2还原CuO所得红色固体Cu中是否含有Cu2O(红色),进行了认真的研究.请你一起踏上探究之路,回答下列问题.
定性和定量结合既是化学的重要思想,也是研究物质组成的重要方法.某研究性学习小组为检测实验室用H2还原CuO所得红色固体Cu中是否含有Cu2O(红色),进行了认真的研究.请你一起踏上探究之路,回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com