
科目: 来源: 题型:解答题
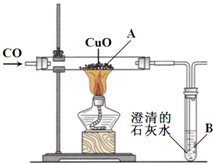 图为一氧化碳还原氧化铜的装置图:
图为一氧化碳还原氧化铜的装置图:查看答案和解析>>
科目: 来源: 题型:解答题
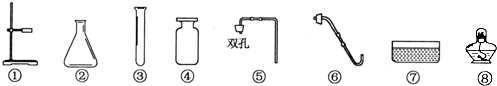
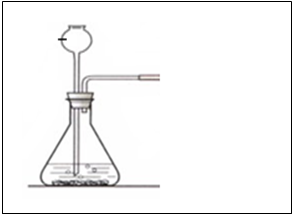
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 铁在氧气中燃烧:2Fe+3O2=2Fe2O3 | |
| B. | 生石灰可与水反应生成氢氧化钙CaO+H2O═Ca(OH)2 | |
| C. | 洗去试管壁上附着的铜Cu+H2SO4═CuSO4+H2↑ | |
| D. | 炼铁高炉中发生的主要反应2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+2CO2↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 发现天然气泄漏时,应立即关闭阀门、开窗通风,不触动电器开关 | |
| B. | 雨水淋湿自行车后,必须先用干布擦净后才能用带油的布擦 | |
| C. | 洗涤剂具有乳化功能,常用来除去餐具上的油污 | |
| D. | 为了使氯化钠从溶液中结晶析出,采用冷却热饱和溶液的方法 |
查看答案和解析>>
科目: 来源: 题型:选择题
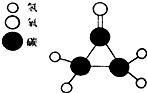 美国科学家在银河星系中央的星云中发现了新的星际分子.星际分子的不断发现可帮助人们了解生命的起源.下列对该分子的叙述中正确的是( )
美国科学家在银河星系中央的星云中发现了新的星际分子.星际分子的不断发现可帮助人们了解生命的起源.下列对该分子的叙述中正确的是( )| A. | 该分子是由碳元素、氢元素和氧元素组成的 | |
| B. | 该分子是由3个碳原子、2个氢原子和1个水分子构成的 | |
| C. | 该一个分子中有8个原子 | |
| D. | 该分子中质子数等于中子数 |
查看答案和解析>>
科目: 来源: 题型:解答题
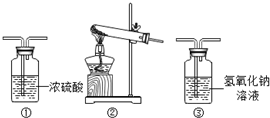 已知:铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它受热分解的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O
已知:铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它受热分解的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O| 装置 质量 时间 | 装置① | 装置③ |
| 实验前 | 220.0克 | 195.0克 |
| 实验后 | 222.1克 | 199.4克 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com