
科目: 来源: 题型:解答题
 甲、乙、丙三种物质均含地壳中含量最多的元素.甲、乙是组成元素相同的化合物,丙是单质;甲、乙在常温下均为液体,在一定条件下均可分解成丙;它们之间有如图所示的转化关系(部分物质和反应条件已经略去).则:
甲、乙、丙三种物质均含地壳中含量最多的元素.甲、乙是组成元素相同的化合物,丙是单质;甲、乙在常温下均为液体,在一定条件下均可分解成丙;它们之间有如图所示的转化关系(部分物质和反应条件已经略去).则:查看答案和解析>>
科目: 来源: 题型:解答题
| 物质名称 | 化学式 | 常温时的状态 |
| 丁烷 | C4H10 | 气 |
| 戊烷 | C5H12 | 液(油状) |
| 癸烷 | C10H22 | 液(油状) |
| 十八烷 | C18H38 | 固 |
| 二十四烷 | C24H50 | 固 |
| 序号 | 实验目的 | 实验操作 | 实验现象 |
| I | 探究哪一层火焰的温度最高 | 点燃蜡烛,把一根火柴梗平放在蜡烛的火焰中,约1s后取出观察 | |
| Ⅱ | 探究焰心中参与燃烧的物质的成分 | 点燃一根较粗的蜡烛,取一根一端为尖嘴的玻璃导管,一端伸入火焰的焰心处,然后在尖嘴一端导管口用火柴点燃 | 导管口处出现火焰 |
| III | 继续探究焰心中参与燃烧的物质的成分 | 点燃一根蜡烛,用一把带有手柄的小刀,将刀尖伸入火焰中最暗的部分,即焰心处,一段时间后取出,冷却,观察刀尖处的现象 | 冷却至室温后,刀尖处有油状液体和固体物质 |
| IV | 用镊子夹住一片白瓷片,将瓷片伸入火焰中最明亮的部分,即内焰处,观察现象 | 白瓷片表面迅速变黑 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验装置 | 实验主要过程 |
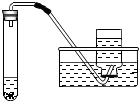 | (1)检验装置气密性.操作如下:先将导管伸入液面下,用手紧握试管,观察到导管口有气泡冒出,松开手后,导管口有液面上升. (2)在试管中依次加入二氧化锰、过碳酸钠和水,有大量气泡生成. (3)收集满一瓶气体. (4)检验气体.方法是将带火星的木条伸入集气瓶里,若带火星的木条复燃,则证明是氧气. |
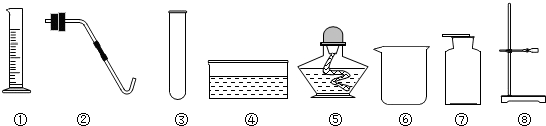
查看答案和解析>>
科目: 来源: 题型:解答题

| A | B | C | |
| 放入苹果起始时间 | 下午2:00 | 下午2:00 | 下午2:00 |
| 实验现象 | 下午2:03 苹果变色 | 下午2:09 苹果变色 | 下午2:19 苹果未变色 |
| A | B | |
| 进入水的体积 | 200mL | 42mL |
| 苹果消耗气体的体积 | 50mL | 8mL |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
 用装置图所示仪器测定空气中O2体积含量,A为标有将容积分成五等份标线的集气瓶,B为固定一燃烧匙的单孔胶塞,烧杯中盛红墨水,通过下列实验步骤,①打开夹子K②点燃匙中红磷③夹紧K夹④将B按进A瓶口,塞紧.回答;
用装置图所示仪器测定空气中O2体积含量,A为标有将容积分成五等份标线的集气瓶,B为固定一燃烧匙的单孔胶塞,烧杯中盛红墨水,通过下列实验步骤,①打开夹子K②点燃匙中红磷③夹紧K夹④将B按进A瓶口,塞紧.回答;查看答案和解析>>
科目: 来源: 题型:解答题
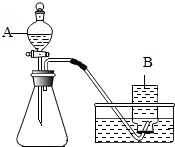 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
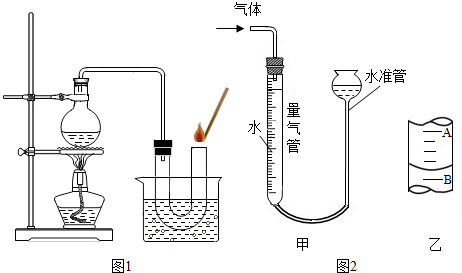
| 同学序号 | 质量分数相同的H2O2溶液 | 溶液中加入的物质 | 收集到的气体体积 |
| 小明 | 100mL | 未加其他物质 | a mL |
| 小李 | 100mL | Fe2O3 0.5g | b mL |
| 小张 | 100mL | MnO2 0.5g | c mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com