3.实验室制取气体所需装置如图Ⅰ所示.请回答以下问题:
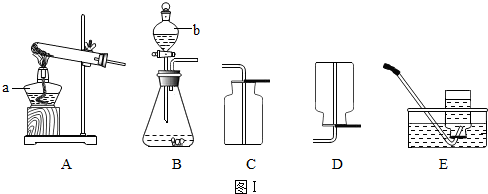
(1)装置中标“a”的仪器名称是酒精灯,标“b”的仪器名称是分液漏斗.
(2)用高锰酸钾制取并收集一瓶的氧气,发生反应的符号表达式为2KMnO
4$\frac{\underline{\;\;△\;\;}}{\;}$K
2MnO
4+MnO
2+O
2↑,所选用的发生装置是A(填字母序号,下同),收集装置是E或C.当用E方法收集O
2,收集满并取出集气瓶后,停止该实验的正确操作方法是先撤出导管,再熄灭酒精灯.
(3)利用如图装置(夹持装置未画出)能进行的实验是B.
A.用高锰酸钾制氧气
B.用双氧水与二氧化锰制氧气
C.用石灰石与稀盐酸制二氧化碳
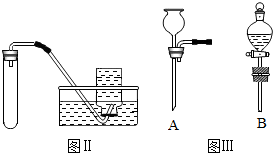
(4)图Ⅱ中的气体发生装置虽然简单,操作方便,但无法控制反应速率.请从图Ⅲ中选取B(选填序号)与图Ⅱ组装成新的气体发生装置,以达到控制反应速率的目的.
(5)催化剂在生产、生活和科研中的地位越来越重要.实验室用过氧化氢溶液分解制取氧气时,就常用二氧化锰作催化剂.
【提出问题】红砖粉能作过氧化氢分解的催化剂吗?
【提出猜想】甲同学认为红砖粉可以代替MnO
2作过氧化氢溶液分解的催化剂.
【设计实验】
①在试管中加入10mL6%的过氧化氢溶液,将带火星的木条伸入试管中;
②准确称量0.5g红砖粉,并放入另一支试管中,将带火星的木条伸入试管中;
③在步骤②的试管中加入10mL 6%过氧化氢溶液,将带火星木条伸入试管中;
④待步骤③的试管中无气泡冒出后,经过操作A、洗涤、干燥、称量得粉末仍为0.5g;
⑤另取10mL6%过氧化氢溶液,加入步骤④中所得固体,将带火星木条伸入试管.
【问题讨论】
a.步骤①中的现象为带火星的木条不复燃,步骤③、⑤中带火星的木条复燃.
b.步骤④中操作A的名称是过滤.若提供了铁架台、玻璃棒、烧杯还缺少的玻璃仪器为漏斗,其中玻璃棒的作用为引流.
c.步骤①和步骤③的操作目的是对比.
d.步骤⑤实验的目的为探究红砖粉的化学性质是否改变.
【实验结论】:红砖粉能作过氧化氢分解的催化剂.



 如图,硒被誉为“抗癌大王”.根据提供的硒的有关信息,下列说法中,正确的是( )
如图,硒被誉为“抗癌大王”.根据提供的硒的有关信息,下列说法中,正确的是( )