
科目: 来源: 题型:选择题
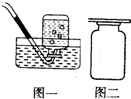
| A. | 密度比空气小,难溶于水 | B. | 密度比空气小,可溶于水 | ||
| C. | 密度比空气大,难溶于水 | D. | 密度比空气大,可溶于水 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 是一种混合物 | B. | 具有导电性 | C. | 不与酸反应 | D. | 具有可燃性 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
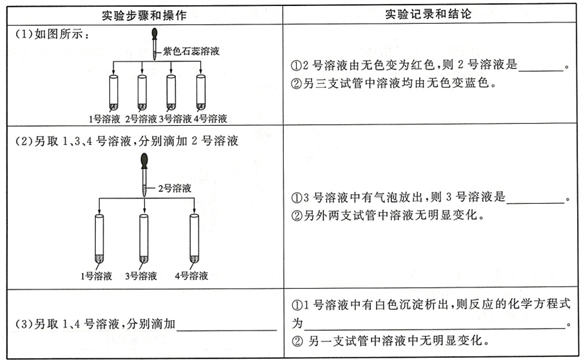
| 实验操作 | 实验现象 | 实验结论 |
| 任取三种溶液于三支试管中,分别滴加第四种溶液 | ①一支试管中有气泡放出,其余两支试管中无明显变化 | ①第四种溶液为稀盐酸 |
| ②一支试管中有白色沉淀析出,其余两支试管中溶液无明显变化 | ③第四种为Na2CO3溶液 | |
| ④三支试管中溶液均无明显变化 | ②第四种为NaOH溶液 |
查看答案和解析>>
科目: 来源: 题型:解答题
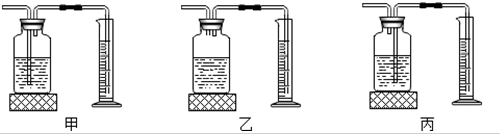
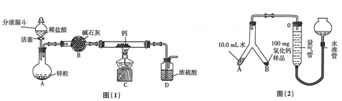
 小明同学在“金属拓展阅读”活动中了解到:金属钠在常温下与水剧烈反应能生成一种可燃性气体.教师结合小明已有知识设计了如图所示装置进行实验.
小明同学在“金属拓展阅读”活动中了解到:金属钠在常温下与水剧烈反应能生成一种可燃性气体.教师结合小明已有知识设计了如图所示装置进行实验.| 操作 | 现象及解释 | |
| ① | 打开止水夹a及分液漏斗活塞,待液体充满大试管后,关闭止水夹a及分液漏斗活塞. | 液体分层,钠熔成银白色小球,在液体分层的界面上方跳动,产生大量气泡,下层溶液变成红色,并逐渐被压入B中.金属钠的物理性质:银白色、熔点低、密度小于水的密度(或大于煤油). |
| ② | 打开止水夹b,待B中部分溶液进入C中,迅速关闭止水夹b. | 反应的化学方程式为CO2+2NaOH═Na2CO3+H2O. |
| ③ | 打开止水夹c | 反应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
| ④ | 将燃着的木条伸到导管尖嘴处,打开止水夹a; 在火焰上方罩一个干冷的烧杯. | 气体燃烧,产生淡蓝色火焰 烧杯内壁有无色液滴生成,A中气体为氢气. |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验操作 | 实验现象 |
| 想两个充满SO2的200mL,软塑料瓶中分别注入10mL的水喝NaOH溶液,振荡,对比 | 两个瓶子变瘪的程度完全相同 |
| 实验操作 | 实验现象 |
 利用如图所示装置分别进行实验,向两个充满SO2的300mL集气瓶中分别加入6mL水和NaOH溶液,一段时间后,打开止水夹,对比 利用如图所示装置分别进行实验,向两个充满SO2的300mL集气瓶中分别加入6mL水和NaOH溶液,一段时间后,打开止水夹,对比 | 倒吸入两个集气瓶中的液体体积完全相同 |
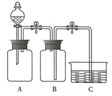 丁同学思考后,将上述装置进行了改进,便达到实验目的.改进装置如图所示,你认为装置B的作用是防止水倒吸入装置A.
丁同学思考后,将上述装置进行了改进,便达到实验目的.改进装置如图所示,你认为装置B的作用是防止水倒吸入装置A.| 实验目的 | 实验步骤 | 实验现象 | 化学方程式和实验结论 |
| 探究所用澄清石灰水是否变质 | ①用一支试管另取少量澄清石灰水 ②取稀硫酸与碳酸钠反应制取CO2 ③将产生的气体通入所用澄清石灰水中 | 步骤③中的实验现象为:石灰水变浑浊或未变浑浊 | 步骤②中反应方程式为H2SO4+Na2CO3=Na2SO4+H2O+CO2↑ 实验结论:所用澄清石灰水没有变质 或所用澄清石灰水已变质 |
| 实验目的 | 实验步骤 | 实验现象 | 化学方程式和实验结论 |
| 探究气体X中是否含有HCl气体 | 将气体X通入硝酸银溶液 | 硝酸银溶液变浑浊 | 反应方程式:HCl+AgNO3=AgCl↓+HNO3 实验结论:气体X中含有氯化氢气体 |
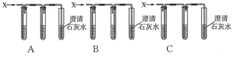
查看答案和解析>>
科目: 来源: 题型:解答题
| 名称 | 食用纯碱 | 食用小苏打 |
| 主要成分 | Na2CO3 | NaHCO3 |
| 酸碱性 | 水溶液呈碱性 | 水溶液呈碱性 |
| 热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
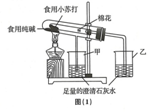 (1)为确保安全,实验结束时,在撤离酒精灯前必须完成的操作是把A、B试管中的导管移出液面.
(1)为确保安全,实验结束时,在撤离酒精灯前必须完成的操作是把A、B试管中的导管移出液面.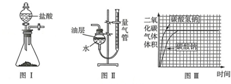
查看答案和解析>>
科目: 来源: 题型:解答题
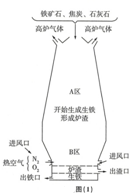 钢铁工业是国家工业的基础.
钢铁工业是国家工业的基础.
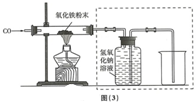
| 物质 性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com