
科目: 来源: 题型:选择题
| A. | 溶质守恒--溶液在稀释前后溶质的体积不变 | |
| B. | 质量守恒--参加反应的各物质的质量总和等于生成的各物质的质量总和 | |
| C. | 元素守恒--化学反应前后元素的种类和质量不变 | |
| D. | 原子守恒--化学反应前后原子的种类及数目不变 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
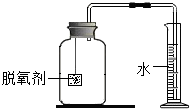
查看答案和解析>>
科目: 来源: 题型:解答题
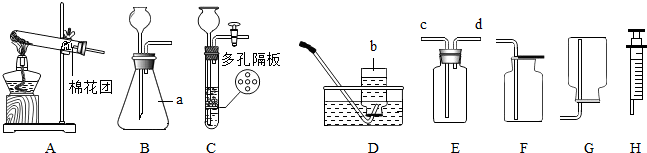
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 生成的气体一定是过氧化氢分解产生的氢气 | |
| B. | 伤口处的生物酶可能对过氧化氢的分解起到催化作用 | |
| C. | 只有二氧化锰能使过氧化氢在常温下迅速分解 | |
| D. | 过氧化氢中氧元素的化合价为负二价 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氢气和液氢都可做燃料--相同物质的分子,其化学性质相同 | |
| B. | 桂花盛开花香四溢--分子在不断运动 | |
| C. | 用水银温度计测量体温--温度升高,原子间空隙变大 | |
| D. | 水烧开后易把壶盖冲起--温度升高,分子变大 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com