
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 次氯酸钠中氯元素的化合价为-1 | |
| B. | 次氯酸钠是氧化物 | |
| C. | 过氧乙酸由三个元素组成 | |
| D. | 过氧乙酸中碳、氢、氧元素的原子个数比为2:4:3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2Cu中的“2”表示2个铜分子 | |
| B. | Mg2+中的“2”表示每个镁离子带有2个单位的正电荷 | |
| C. | H2S中的“2”表示硫化氢分子中含有2个氢原子 | |
| D. | H2O中的“2”表示一个水分子中含有2个氢元素 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 称氯化钠固体时,物码颠倒并使用游码 | |
| B. | 用量筒量水时,面对刻度俯视凹页面的最低处读数 | |
| C. | 将量筒内的水倒入烧杯时,有水溅出 | |
| D. | 将配好的溶液倒入细口瓶时,不慎洒落 |
查看答案和解析>>
科目: 来源: 题型:解答题
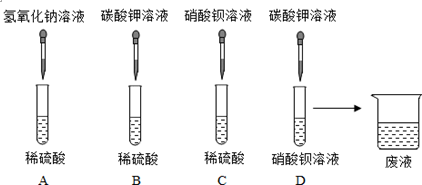
 .
.| 溶液中可能含有离子 | 实验步骤 | 实验现象 | 实验结论 |
| ①可能含有 Ba2+ | ②取滤液滴加 硫酸钠溶液 | 现象明显 | 含有该离子 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
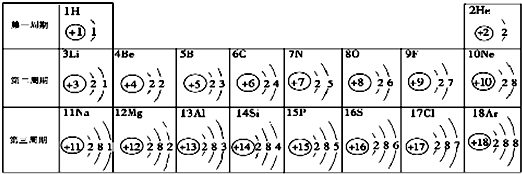
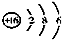 ,离子符号是S2-,该元素的原子核外有3个电子层,它属于非金属元素(填“金属”、“非金属”),其化学性质比较活泼,在化学反应中易得到(填“得到”、“失去”)电子.
,离子符号是S2-,该元素的原子核外有3个电子层,它属于非金属元素(填“金属”、“非金属”),其化学性质比较活泼,在化学反应中易得到(填“得到”、“失去”)电子.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com