
科目: 来源:石家庄新世纪外国语学校2017-2018年度九年级第一学期第三次质量检测化学试卷 题型:单选题
下列关于溶液的说法中正确的是( )
A. 水可以溶解任何物质
B. 物质溶于水时都放出热量
C. 溶质可以是固体,也可以是液体或气体
D. 饱和溶液就是不能再溶解任何物质的溶液
【答案】C
【解析】水是常见的溶剂,但不是任何物质都能溶于水,如碳酸钙、植物油都不能溶于水,A错误.物质溶于水时,有的表现为放热,如浓硫酸;有的表现为吸热,如硝酸铵;有的温度几乎不变,如氯化钠,B错误.一种溶质的饱和溶液不能再溶解该物质,但还可以溶解其他物质,如氯化钠的饱和溶液还可以溶解高锰酸钾,D错误.
【题型】单选题
【结束】
23
20℃时,取甲、乙、丙、丁四种纯净物各20g,分别加入到四个各盛有50g水的烧杯中,充分溶解,其溶解情况如下表:
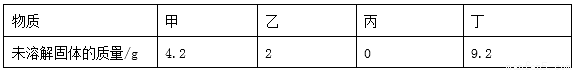
下列说法正确的是( )
A. 所得四杯溶液都是饱和溶液
B. 丁溶液中溶质的质量最大
C. 20℃时四种物质溶解度的关系为:丙>乙>甲>丁
D. 四杯溶液中溶剂的质量大小为:丙溶液>乙溶液>甲溶液>丁溶液
【答案】C
【解析】A、丙物质未溶解的固体的质量为0可知丙溶液可能为饱和溶液,也可能为不饱和溶液,错误;B、溶剂质量相同而丁溶液的溶质质量最小,所以丁溶液的溶质质量分数最小,错误;C、溶剂质量相同而甲、乙、丙、丁四种溶液中溶质质量的大小关系为丙>乙>甲>丁,所以20℃时四种物质溶解度的关系为:丙>乙>甲>丁,正确;D、四杯溶液中溶剂的质量都为50g,错误。答案C。
【题型】单选题
【结束】
24
20 ℃时氯化钾的溶解度为34 g。下列是四位同学在20 ℃时配制的氯化钾溶液,其中一定达到饱和的是( )
A. 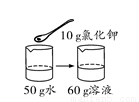 B.
B. 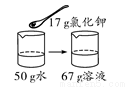 C.
C.  D.
D. 
查看答案和解析>>
科目: 来源:石家庄新世纪外国语学校2017-2018年度九年级第一学期第三次质量检测化学试卷 题型:单选题
20℃时,取甲、乙、丙、丁四种纯净物各20g,分别加入到四个各盛有50g水的烧杯中,充分溶解,其溶解情况如下表:
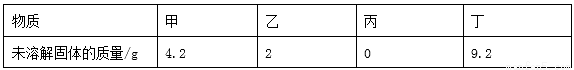
下列说法正确的是( )
A. 所得四杯溶液都是饱和溶液
B. 丁溶液中溶质的质量最大
C. 20℃时四种物质溶解度的关系为:丙>乙>甲>丁
D. 四杯溶液中溶剂的质量大小为:丙溶液>乙溶液>甲溶液>丁溶液
【答案】C
【解析】A、丙物质未溶解的固体的质量为0可知丙溶液可能为饱和溶液,也可能为不饱和溶液,错误;B、溶剂质量相同而丁溶液的溶质质量最小,所以丁溶液的溶质质量分数最小,错误;C、溶剂质量相同而甲、乙、丙、丁四种溶液中溶质质量的大小关系为丙>乙>甲>丁,所以20℃时四种物质溶解度的关系为:丙>乙>甲>丁,正确;D、四杯溶液中溶剂的质量都为50g,错误。答案C。
【题型】单选题
【结束】
24
20 ℃时氯化钾的溶解度为34 g。下列是四位同学在20 ℃时配制的氯化钾溶液,其中一定达到饱和的是( )
A. 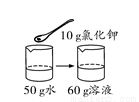 B.
B. 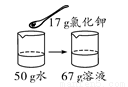 C.
C. 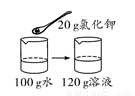 D.
D. 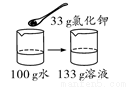
【答案】B
【解析】A、20℃时氯化钾的溶解度为34g,含义是20℃时,100g水中最多能溶解氯化钾34g,溶液达到饱和状态,则20℃时,50g水中最多能溶解氯化钾17g,溶液达到饱和状态,向50g水中加入10g氯化钾,所得溶液是不饱和溶液,错误;B、20℃时氯化钾的溶解度为34g,含义是20℃时,100g水中最多能溶解氯化钾34g,溶液达到饱和状态,则20℃时,50g水中最多能溶解氯化钾17g,溶液达到饱和状态,向50g水中加入17g氯化钾,所得溶液是恰好是饱和溶液,正确;C、20℃时氯化钾的溶解度为34g,含义是20℃时,100g水中最多能溶解氯化钾34g,溶液达到饱和状态,20℃时,向100g水中加入20g氯化钾,所得溶液是不饱和溶液,错误;D、20℃时氯化钾的溶解度为34g,含义是20℃时,100g水中最多能溶解氯化钾34g,溶液达到饱和状态,20℃时,向100g水中加入33g氯化钾,所得溶液是不饱和溶液,错误。故选B。
【题型】单选题
【结束】
25
要将一瓶接近饱和的石灰水变成饱和溶液,小明选择了如下方法.其中可行的是( )
①加入CaO
②加入Ca(OH)2
③升高温度
④降低温度
A.②③ B.②④ C.①②③ D.①②④
查看答案和解析>>
科目: 来源:石家庄新世纪外国语学校2017-2018年度九年级第一学期第三次质量检测化学试卷 题型:单选题
20 ℃时氯化钾的溶解度为34 g。下列是四位同学在20 ℃时配制的氯化钾溶液,其中一定达到饱和的是( )
A. 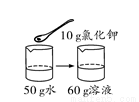 B.
B. 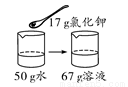 C.
C. 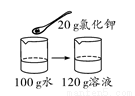 D.
D. 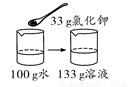
【答案】B
【解析】A、20℃时氯化钾的溶解度为34g,含义是20℃时,100g水中最多能溶解氯化钾34g,溶液达到饱和状态,则20℃时,50g水中最多能溶解氯化钾17g,溶液达到饱和状态,向50g水中加入10g氯化钾,所得溶液是不饱和溶液,错误;B、20℃时氯化钾的溶解度为34g,含义是20℃时,100g水中最多能溶解氯化钾34g,溶液达到饱和状态,则20℃时,50g水中最多能溶解氯化钾17g,溶液达到饱和状态,向50g水中加入17g氯化钾,所得溶液是恰好是饱和溶液,正确;C、20℃时氯化钾的溶解度为34g,含义是20℃时,100g水中最多能溶解氯化钾34g,溶液达到饱和状态,20℃时,向100g水中加入20g氯化钾,所得溶液是不饱和溶液,错误;D、20℃时氯化钾的溶解度为34g,含义是20℃时,100g水中最多能溶解氯化钾34g,溶液达到饱和状态,20℃时,向100g水中加入33g氯化钾,所得溶液是不饱和溶液,错误。故选B。
【题型】单选题
【结束】
25
要将一瓶接近饱和的石灰水变成饱和溶液,小明选择了如下方法.其中可行的是( )
①加入CaO
②加入Ca(OH)2
③升高温度
④降低温度
A.②③ B.②④ C.①②③ D.①②④
【答案】C
【解析】
试题分析:向接近饱和的溶液中增加溶质或蒸发溶剂都可以使溶液变成饱和溶液,故把一瓶接近饱和的石灰水变成饱和,①加入CaO,氧化钙与水反应生成氢氧化钙,②加入氢氧化钙,使溶液中的溶质增多。①②均能将一瓶接近饱和的石灰水变成饱和溶液。由于氢氧化钙的溶解度随温度升高而减小,升高温度后氢氧化钙的溶解度变小,故把一瓶接近饱和的石灰水变成饱和,还可以采取③升高温度的方法。故①②③符合题意,正确选项是C。
考点:考查饱和溶液和不饱和溶液相互转变的方法的知识。
【题型】单选题
【结束】
26
甲、乙两种物质的溶解度曲线如下图所示,下列说法正确的是( )
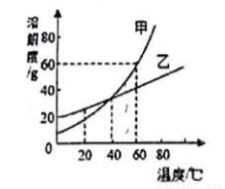
A. 20℃时,甲的溶解度比乙大
B. 60℃的,甲、乙两物质的饱和溶液温度降低到t1℃时析出晶体甲比乙多
C. 40℃的,甲的饱和溶液升温到60℃仍是饱和溶液
D. 60℃时,在70g的甲中加入100g的水,甲不能完全溶解
查看答案和解析>>
科目: 来源:石家庄新世纪外国语学校2017-2018年度九年级第一学期第三次质量检测化学试卷 题型:单选题
要将一瓶接近饱和的石灰水变成饱和溶液,小明选择了如下方法.其中可行的是( )
①加入CaO
②加入Ca(OH)2
③升高温度
④降低温度
A.②③ B.②④ C.①②③ D.①②④
【答案】C
【解析】
试题分析:向接近饱和的溶液中增加溶质或蒸发溶剂都可以使溶液变成饱和溶液,故把一瓶接近饱和的石灰水变成饱和,①加入CaO,氧化钙与水反应生成氢氧化钙,②加入氢氧化钙,使溶液中的溶质增多。①②均能将一瓶接近饱和的石灰水变成饱和溶液。由于氢氧化钙的溶解度随温度升高而减小,升高温度后氢氧化钙的溶解度变小,故把一瓶接近饱和的石灰水变成饱和,还可以采取③升高温度的方法。故①②③符合题意,正确选项是C。
考点:考查饱和溶液和不饱和溶液相互转变的方法的知识。
【题型】单选题
【结束】
26
甲、乙两种物质的溶解度曲线如下图所示,下列说法正确的是( )
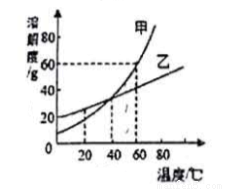
A. 20℃时,甲的溶解度比乙大
B. 60℃的,甲、乙两物质的饱和溶液温度降低到t1℃时析出晶体甲比乙多
C. 40℃的,甲的饱和溶液升温到60℃仍是饱和溶液
D. 60℃时,在70g的甲中加入100g的水,甲不能完全溶解
【答案】D
【解析】A、通过分析溶解度曲线可知,20℃时,甲的溶解度比乙小,错误;B、不知饱和溶液的质量,无法判断析出晶体质量多少,若二者饱和溶液的质量相等,60℃的甲、乙两物质的饱和溶液温度降低到t1℃时析出晶体甲比乙多,错误;C、甲的溶解度随温度的升高而增大,40℃时,甲的饱和溶液升温到60℃会变为不饱和溶液,错误;D、60℃时,甲的溶解度为60g,60℃时,100g水中最多溶解60g 甲,在70g的甲中加入100g的水,甲不能完全溶解,正确。故选D。
【题型】单选题
【结束】
27
根据下图所示的溶解度曲线判断,下列说法正确的是( )

A. 甲物质的溶解度大于乙物质的溶解度
B. 甲物质的不饱和溶液温度升高后变成饱和溶液
C. t2℃时,甲物质的饱和溶液和乙物质的饱和溶液中含有相等质量的溶质
D. 将t2℃甲、乙两物质的饱和溶液温度降低到t1℃时都会析出晶体
查看答案和解析>>
科目: 来源:石家庄新世纪外国语学校2017-2018年度九年级第一学期第三次质量检测化学试卷 题型:单选题
甲、乙两种物质的溶解度曲线如下图所示,下列说法正确的是( )
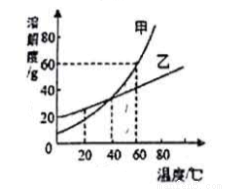
A. 20℃时,甲的溶解度比乙大
B. 60℃的,甲、乙两物质的饱和溶液温度降低到t1℃时析出晶体甲比乙多
C. 40℃的,甲的饱和溶液升温到60℃仍是饱和溶液
D. 60℃时,在70g的甲中加入100g的水,甲不能完全溶解
【答案】D
【解析】A、通过分析溶解度曲线可知,20℃时,甲的溶解度比乙小,错误;B、不知饱和溶液的质量,无法判断析出晶体质量多少,若二者饱和溶液的质量相等,60℃的甲、乙两物质的饱和溶液温度降低到t1℃时析出晶体甲比乙多,错误;C、甲的溶解度随温度的升高而增大,40℃时,甲的饱和溶液升温到60℃会变为不饱和溶液,错误;D、60℃时,甲的溶解度为60g,60℃时,100g水中最多溶解60g 甲,在70g的甲中加入100g的水,甲不能完全溶解,正确。故选D。
【题型】单选题
【结束】
27
根据下图所示的溶解度曲线判断,下列说法正确的是( )
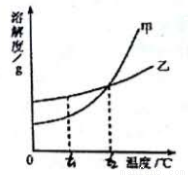
A. 甲物质的溶解度大于乙物质的溶解度
B. 甲物质的不饱和溶液温度升高后变成饱和溶液
C. t2℃时,甲物质的饱和溶液和乙物质的饱和溶液中含有相等质量的溶质
D. 将t2℃甲、乙两物质的饱和溶液温度降低到t1℃时都会析出晶体
【答案】D
【解析】A、由于固体物质的溶解度会随温度的变化而变化,从图中可以看出,只有在高于t2℃时,甲的溶解度大于乙的溶解度,错误;B、甲的溶解度随着温度的升高而增大,物质甲的不饱和溶液温度升高后仍为不饱和溶液,错误;C、由于甲乙两饱和溶液的质量不一定相等,故无法比较所含溶质的质量,错误;D、甲乙的溶解度都随着温度的降低而减小,故将t2℃甲、乙两物质的饱和溶液温度降低到t1℃时都会析出晶体,正确。故选C。
点睛:对于溶解度的意义的表达一般有两种方式:一种是在某温度时,100g水里最多能溶解多少克某物质;另一种是在某温度时,100g水里溶解多少克某物质,溶液达到饱和状态。
【题型】单选题
【结束】
28
将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如下图所示。根据图中所提供的信息,得出的结论正确的是( )(A、B、C在生成物中均为+2价)

A. 消耗稀盐酸的质量是:A>B>C B. 金属活动性顺序是A>B>C
C. 反应速率最快的是A D. 相对原子质量的大小关系是A>B>C
查看答案和解析>>
科目: 来源:石家庄新世纪外国语学校2017-2018年度九年级第一学期第三次质量检测化学试卷 题型:单选题
根据下图所示的溶解度曲线判断,下列说法正确的是( )
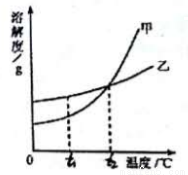
A. 甲物质的溶解度大于乙物质的溶解度
B. 甲物质的不饱和溶液温度升高后变成饱和溶液
C. t2℃时,甲物质的饱和溶液和乙物质的饱和溶液中含有相等质量的溶质
D. 将t2℃甲、乙两物质的饱和溶液温度降低到t1℃时都会析出晶体
【答案】D
【解析】A、由于固体物质的溶解度会随温度的变化而变化,从图中可以看出,只有在高于t2℃时,甲的溶解度大于乙的溶解度,错误;B、甲的溶解度随着温度的升高而增大,物质甲的不饱和溶液温度升高后仍为不饱和溶液,错误;C、由于甲乙两饱和溶液的质量不一定相等,故无法比较所含溶质的质量,错误;D、甲乙的溶解度都随着温度的降低而减小,故将t2℃甲、乙两物质的饱和溶液温度降低到t1℃时都会析出晶体,正确。故选C。
点睛:对于溶解度的意义的表达一般有两种方式:一种是在某温度时,100g水里最多能溶解多少克某物质;另一种是在某温度时,100g水里溶解多少克某物质,溶液达到饱和状态。
【题型】单选题
【结束】
28
将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如下图所示。根据图中所提供的信息,得出的结论正确的是( )(A、B、C在生成物中均为+2价)

A. 消耗稀盐酸的质量是:A>B>C B. 金属活动性顺序是A>B>C
C. 反应速率最快的是A D. 相对原子质量的大小关系是A>B>C
【答案】A
【解析】A、根据质量守恒定律可知,氢元素全部来自酸,生成氢气的质量A>B>C,所以消耗稀盐酸的质量是A>B>C,正确;B、根据反应生成H2的质量与反应时间的关系图所示,当三种金属都在发生反应时,相同时间内B放出氢气的质量大于A、大于C,可判断三种金属中B的活动性最强;错误;C、根据反应生成H2的质量与反应时间的关系图所示,等质量的三种金属B最先完全反应,因此反应速度最大的是B而不是A;错误;D、三种金属的化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;根据反应生成H2的质量与反应时间的关系图所示,在三种金属完全反应后,放出H2的质量是A>B>C;因此可判断相对原子质量是C>B>A,错误。故选A。
点睛:对于活泼金属,活动性越强的金属与酸反应越剧烈,即反应放出氢气的速度越快;化合价相同的等质量金属完全反应放出氢气的质量与金属的相对原子质量成反比。
【题型】单选题
【结束】
29
将等质量的镁、铁、锌分别放入三份溶质质量分数相同的稀盐酸中,反应生成的H2的质量与反应时间的关系如图所示.根据图中的信息,作出的判断不正确的是( )

A. 图线X表示镁的反应情况
B. 铁消耗的稀盐酸的质量最大
C. 镁、锌一定过量,铁可能反应完
D. 镁一定过量,锌、铁可能反应完
查看答案和解析>>
科目: 来源:石家庄新世纪外国语学校2017-2018年度九年级第一学期第三次质量检测化学试卷 题型:null
将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如下图所示。根据图中所提供的信息,得出的结论正确的是( )(A、B、C在生成物中均为+2价)

A. 消耗稀盐酸的质量是:A>B>C B. 金属活动性顺序是A>B>C
C. 反应速率最快的是A D. 相对原子质量的大小关系是A>B>C
【答案】A
【解析】A、根据质量守恒定律可知,氢元素全部来自酸,生成氢气的质量A>B>C,所以消耗稀盐酸的质量是A>B>C,正确;B、根据反应生成H2的质量与反应时间的关系图所示,当三种金属都在发生反应时,相同时间内B放出氢气的质量大于A、大于C,可判断三种金属中B的活动性最强;错误;C、根据反应生成H2的质量与反应时间的关系图所示,等质量的三种金属B最先完全反应,因此反应速度最大的是B而不是A;错误;D、三种金属的化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;根据反应生成H2的质量与反应时间的关系图所示,在三种金属完全反应后,放出H2的质量是A>B>C;因此可判断相对原子质量是C>B>A,错误。故选A。
点睛:对于活泼金属,活动性越强的金属与酸反应越剧烈,即反应放出氢气的速度越快;化合价相同的等质量金属完全反应放出氢气的质量与金属的相对原子质量成反比。
【题型】单选题
【结束】
29
将等质量的镁、铁、锌分别放入三份溶质质量分数相同的稀盐酸中,反应生成的H2的质量与反应时间的关系如图所示.根据图中的信息,作出的判断不正确的是( )

A. 图线X表示镁的反应情况
B. 铁消耗的稀盐酸的质量最大
C. 镁、锌一定过量,铁可能反应完
D. 镁一定过量,锌、铁可能反应完
【答案】C
【解析】试题分析:根据金属活动性顺序可知A、图中X反应速度最快,说明X是三种金属中活动性最强的镁;所以判断正确; B、图中铁生成氢气最多,根据反应前后元素质量不变,可判断铁消耗盐酸质量最大;所以判断正确; C、图中镁、锌产生氢气质量相等,说明镁没有完全反应,但不能确定锌也没有完全反应;所以判断错误; D、质量相等的锌、铁完全反应产生氢气的质量关系为:铁>锌,与图中关系一致,可推测锌、铁可能完全反应.所以判断正确;故选C.
考点:金属的性质、金属活动性顺序
【题型】单选题
【结束】
30
向AgNO3溶液中加入一定量的Mg粉和Cu粉,充分反应后过滤,得到滤渣和蓝色的滤液.关于该滤渣和滤液有下列四种说法:①向滤渣中加入稀盐酸,可能有气泡产生;②向滤液中加入稀盐酸一定有沉淀产生;③滤渣中一定有Ag;④滤液中一定有Cu(NO3)2、一定不含AgNO3、可能有Mg(NO3)2,以上说法中正确的个数为( )
A. 1个 B. 2个 C. 3个 D. 4个
查看答案和解析>>
科目: 来源:石家庄新世纪外国语学校2017-2018年度九年级第一学期第三次质量检测化学试卷 题型:填空题
将等质量的镁、铁、锌分别放入三份溶质质量分数相同的稀盐酸中,反应生成的H2的质量与反应时间的关系如图所示.根据图中的信息,作出的判断不正确的是( )

A. 图线X表示镁的反应情况
B. 铁消耗的稀盐酸的质量最大
C. 镁、锌一定过量,铁可能反应完
D. 镁一定过量,锌、铁可能反应完
【答案】C
【解析】试题分析:根据金属活动性顺序可知A、图中X反应速度最快,说明X是三种金属中活动性最强的镁;所以判断正确; B、图中铁生成氢气最多,根据反应前后元素质量不变,可判断铁消耗盐酸质量最大;所以判断正确; C、图中镁、锌产生氢气质量相等,说明镁没有完全反应,但不能确定锌也没有完全反应;所以判断错误; D、质量相等的锌、铁完全反应产生氢气的质量关系为:铁>锌,与图中关系一致,可推测锌、铁可能完全反应.所以判断正确;故选C.
考点:金属的性质、金属活动性顺序
【题型】单选题
【结束】
30
向AgNO3溶液中加入一定量的Mg粉和Cu粉,充分反应后过滤,得到滤渣和蓝色的滤液.关于该滤渣和滤液有下列四种说法:①向滤渣中加入稀盐酸,可能有气泡产生;②向滤液中加入稀盐酸一定有沉淀产生;③滤渣中一定有Ag;④滤液中一定有Cu(NO3)2、一定不含AgNO3、可能有Mg(NO3)2,以上说法中正确的个数为( )
A. 1个 B. 2个 C. 3个 D. 4个
【答案】A
【解析】①充分反应后过滤,得到滤渣和蓝色的滤液,说明镁已经完全反应,铜和硝酸银反应生成了硝酸铜,向滤渣中加入稀盐酸,不可能有气泡产生,错误;②铜和硝酸银反应时,如果硝酸银有剩余,向滤液中加入稀盐酸一定有沉淀产生,如果硝酸银没有剩余,则向滤液中加入稀盐酸没有沉淀产生,错误;③滤渣中一定有Ag,正确;④滤液中一定有Cu(NO3)2、可能含AgNO3、一定有Mg(NO3)2,错误。故选A。
【题型】null
【结束】
31
化学来源于生活,服务于杜会,在生活中蕴藏着许多化学知识。
(1)石家庄市已完成“天然气置换工程”,用天然气代替煤气更有利于保护环境,请写出天然气燃烧的化学方程式____;
(2)“共享单车”由于符合“低碳出行”的理念,现已风靡石家庄,尤其颇受年轻人的喜爱,“低碳出行”中“低碳“指的是较低的______气体排放:如下图所示自行车中的材料属于金属材料的是______(选填序号①、②、③),为防止“共享单车”钢丝网篓锈蚀,可采取的措施有_________(写一种即可)。

(3)碘酒杀菌中的的“酒”指________(用化学式表示);
(4)用洗洁精洗去餐具上的油污,是利用了洗洁精的______作用。
查看答案和解析>>
科目: 来源:石家庄新世纪外国语学校2017-2018年度九年级第一学期第三次质量检测化学试卷 题型:实验题
向AgNO3溶液中加入一定量的Mg粉和Cu粉,充分反应后过滤,得到滤渣和蓝色的滤液.关于该滤渣和滤液有下列四种说法:①向滤渣中加入稀盐酸,可能有气泡产生;②向滤液中加入稀盐酸一定有沉淀产生;③滤渣中一定有Ag;④滤液中一定有Cu(NO3)2、一定不含AgNO3、可能有Mg(NO3)2,以上说法中正确的个数为( )
A. 1个 B. 2个 C. 3个 D. 4个
【答案】A
【解析】①充分反应后过滤,得到滤渣和蓝色的滤液,说明镁已经完全反应,铜和硝酸银反应生成了硝酸铜,向滤渣中加入稀盐酸,不可能有气泡产生,错误;②铜和硝酸银反应时,如果硝酸银有剩余,向滤液中加入稀盐酸一定有沉淀产生,如果硝酸银没有剩余,则向滤液中加入稀盐酸没有沉淀产生,错误;③滤渣中一定有Ag,正确;④滤液中一定有Cu(NO3)2、可能含AgNO3、一定有Mg(NO3)2,错误。故选A。
【题型】null
【结束】
31
化学来源于生活,服务于杜会,在生活中蕴藏着许多化学知识。
(1)石家庄市已完成“天然气置换工程”,用天然气代替煤气更有利于保护环境,请写出天然气燃烧的化学方程式____;
(2)“共享单车”由于符合“低碳出行”的理念,现已风靡石家庄,尤其颇受年轻人的喜爱,“低碳出行”中“低碳“指的是较低的______气体排放:如下图所示自行车中的材料属于金属材料的是______(选填序号①、②、③),为防止“共享单车”钢丝网篓锈蚀,可采取的措施有_________(写一种即可)。

(3)碘酒杀菌中的的“酒”指________(用化学式表示);
(4)用洗洁精洗去餐具上的油污,是利用了洗洁精的______作用。
【答案】 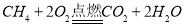 二氧化碳 ②③ 刷漆(其他合理答案均给分)
二氧化碳 ②③ 刷漆(其他合理答案均给分)  乳化
乳化
【解析】本题主要考查了金属锈蚀的条件及其防护,二氧化碳对环境的影响,化学方程式的书写等。
(1)天然气燃烧时生成了水和二氧化碳,化学方程式是 ;
;
(2) “低碳出行”中“低碳”指的是较低的二氧化碳气体排放;自行车中的材料属于金属材料的是钢丝和钛合金,故答案为:②③,为防止“共享单车”钢丝网篓锈蚀,可采取的措施有刷漆;
(3) 碘酒是碘的酒精溶液。碘酒杀菌中的 “酒”指酒精,化学式是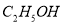 ;
;
(4)用洗洁精洗去餐具上的油污,是利用了洗洁精的乳化作用。
【题型】填空题
【结束】
32
请根据下图的实验装置图回答有关问题;

(1)请写出图中仪器的名称:①_______________。
(2)实验室常用大理石和稀盐酸反应制取二氧化碳,其化学方程式是____。要得到平稳的气流,则应选用__ 发生装置(从A--D中选)。用澄清石灰水可以检验二氧化碳,写出该反应的化学方程式____。
(3)实验室采用A装置(无棉花)制O2的反应方程式为__________。用排水法收集O2,实验刚开始时,水槽里导管的位置较合理的是______(E、F中选择)。
(4)实验室里常用锌粒和稀硫酸反应制取氢气,现发生装置选择D,收集装置选择G。
①与B、C装置相比,选用D作为氢气发生装置的主要优点是__________。
②G装置若用于排空气法收集氢气,氢气应从_________端(选填“a”或“b”)通入。
查看答案和解析>>
科目: 来源:石家庄新世纪外国语学校2017-2018年度九年级第一学期第三次质量检测化学试卷 题型:综合题
化学来源于生活,服务于杜会,在生活中蕴藏着许多化学知识。
(1)石家庄市已完成“天然气置换工程”,用天然气代替煤气更有利于保护环境,请写出天然气燃烧的化学方程式____;
(2)“共享单车”由于符合“低碳出行”的理念,现已风靡石家庄,尤其颇受年轻人的喜爱,“低碳出行”中“低碳“指的是较低的______气体排放:如下图所示自行车中的材料属于金属材料的是______(选填序号①、②、③),为防止“共享单车”钢丝网篓锈蚀,可采取的措施有_________(写一种即可)。

(3)碘酒杀菌中的的“酒”指________(用化学式表示);
(4)用洗洁精洗去餐具上的油污,是利用了洗洁精的______作用。
【答案】 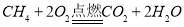 二氧化碳 ②③ 刷漆(其他合理答案均给分)
二氧化碳 ②③ 刷漆(其他合理答案均给分) 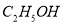 乳化
乳化
【解析】本题主要考查了金属锈蚀的条件及其防护,二氧化碳对环境的影响,化学方程式的书写等。
(1)天然气燃烧时生成了水和二氧化碳,化学方程式是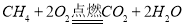 ;
;
(2) “低碳出行”中“低碳”指的是较低的二氧化碳气体排放;自行车中的材料属于金属材料的是钢丝和钛合金,故答案为:②③,为防止“共享单车”钢丝网篓锈蚀,可采取的措施有刷漆;
(3) 碘酒是碘的酒精溶液。碘酒杀菌中的 “酒”指酒精,化学式是 ;
;
(4)用洗洁精洗去餐具上的油污,是利用了洗洁精的乳化作用。
【题型】填空题
【结束】
32
请根据下图的实验装置图回答有关问题;
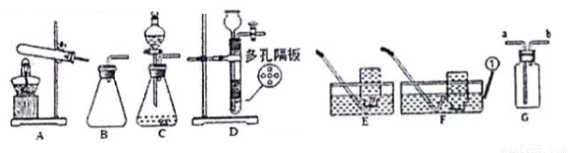
(1)请写出图中仪器的名称:①_______________。
(2)实验室常用大理石和稀盐酸反应制取二氧化碳,其化学方程式是____。要得到平稳的气流,则应选用__ 发生装置(从A--D中选)。用澄清石灰水可以检验二氧化碳,写出该反应的化学方程式____。
(3)实验室采用A装置(无棉花)制O2的反应方程式为__________。用排水法收集O2,实验刚开始时,水槽里导管的位置较合理的是______(E、F中选择)。
(4)实验室里常用锌粒和稀硫酸反应制取氢气,现发生装置选择D,收集装置选择G。
①与B、C装置相比,选用D作为氢气发生装置的主要优点是__________。
②G装置若用于排空气法收集氢气,氢气应从_________端(选填“a”或“b”)通入。
【答案】 水槽  C
C 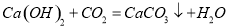 2KC1O3
2KC1O3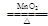 2KC1+3O2↑ F 能随时控制的反应开始和停止 b
2KC1+3O2↑ F 能随时控制的反应开始和停止 b
【解析】考题主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。
(1)图中仪器的名称: 水槽;
(2)大理石和稀盐酸反应生成氯化钙和水和二氧化碳,其化学方程式是 ;C中分液漏斗能控制液体的滴加速率,从而控制反应的速率。要得到平稳的气流,则应选用C发生装置;用澄清石灰水可以检验二氧化碳是考成了碳酸钙和水,该反应的化学方程式是
;C中分液漏斗能控制液体的滴加速率,从而控制反应的速率。要得到平稳的气流,则应选用C发生装置;用澄清石灰水可以检验二氧化碳是考成了碳酸钙和水,该反应的化学方程式是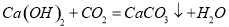 ;
;
(3)实验室采用A装置(无棉花)制O2是用氯酸钾和二氧化锰共热反应生成氯化钾和氧气,反应方程式为 ;刚开始有气泡从导管口冒出,放出的气体有装置中的空气,此时不能开始收集,所以导管位置合理的是F;
;刚开始有气泡从导管口冒出,放出的气体有装置中的空气,此时不能开始收集,所以导管位置合理的是F;
(4)实验室里常用锌粒和稀硫酸反应制取氢气,现发生装置选择D,收集装置选择G。
①与B、C装置相比,选用F作为氢气发生装置的主要优点是能使反应随时进行或停止,原理是:关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止;打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行;
②由于氢气密度比空气小,应从b端通入。
【题型】实验题
【结束】
33
对比实验是化学学习中常用的一种实验方法。
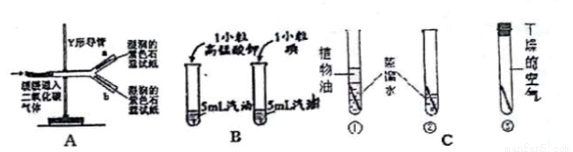
(1)在验证CO2性质时,若把Y形导管固定在铁架台上(如图12中A),a管位于上方,b管位于下方,两条紫色石蕊试纸均湿润,可观察到现象是____,在该实验中验证的CO2化学性质是(用化学方程表示)_____。
(2)图中B实验的目的是_______。
(3)图的C实验中为了得出“铁生锈需要与水接触”这一结论,要选择的对比实验是______。(选填序号①、②、③)
(4)某同学用设计了如下图中所示装置,探究燃烧的条件(瓶1、瓶2充入氧气,瓶3和烧杯中充有80℃热水)。
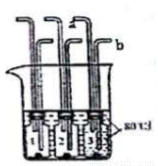
A.瓶1中加入少量白磷,瓶2、瓶3中分别放入____、_____,可同时证明可燃物燃烧的两个条件。
B.若仅利用瓶3证明“与氧气接触”是可燃物燃烧的条件之一,则相应的操作方法是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com