
科目: 来源:安徽省南陵县2018届九年级下学期第一次联考化学试卷 题型:单选题
有X、Y、Z三种金属,其中Y能与稀硫酸反应,而X、Z不能与稀硫酸反应;将Z浸入X的盐溶液中,在Z的表面有X析出.则X、Y、Z的金属活动性由强到弱的顺序是
A. X、Y、Z B. Y、Z、X C. Y、X、Z D. Z、X、Y
B 【解析】Y能与稀硫酸反应产生氢气,而X、Z不能与稀硫酸反应,说明Y的活动性最强,Z浸入X的盐溶液中,Z的表面有X析出,说明Z的活动性比X强,故活动性强弱顺序为:Y、Z、X,故选D。查看答案和解析>>
科目: 来源:安徽省南陵县2018届九年级下学期第一次联考化学试卷 题型:null
如图是镨元素在元素周期表中的部分信息。下列说法中正确的是
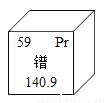
A. 镨元素的元素符号是Pr B. 镨的相对原子质量为140.9g
C. 镨原子的核内中子数为59 D. 镨元素是非金属元素
A 【解析】A.镨元素的元素符号是Pr,故A正确;B.镨的相对原子质量为140.9,没有单位,故B错误;C.镨原子的核内质子数为59,故C错误;D.镨元素是金属元素,故D错误。查看答案和解析>>
科目: 来源:安徽省南陵县2018届九年级下学期第一次联考化学试卷 题型:单选题
甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是

A. 20 ℃时,甲溶液中溶质的质量分数一定比乙溶液的大
B. 将40 ℃时甲的一定量饱和溶液降温至20 ℃,溶液质量不变
C. 甲的溶解度大于乙的溶解度
D. 40 ℃时,分别在100 g水中各加入30 g甲、乙,同时降温至20 ℃,甲、乙溶液均为饱和溶液
D 【解析】A、20 ℃时,甲、乙溶解度相等。但甲、乙溶液是否饱和不确定,故甲溶液不一定比乙溶液浓,错误;B、将40 ℃时甲的一定量饱和溶液降温至20 ℃,有溶质析出,溶液质量变小,错误;C、温度大于20 ℃时,甲的溶解度大于乙的溶解度,错误;D、20 ℃时,甲、乙溶解度相等为30g。40 ℃时,分别在100 g水中各加入30 g甲、乙,同时降温至20 ℃,甲、乙溶液均为饱和溶液,正确。故选...查看答案和解析>>
科目: 来源:安徽省南陵县2018届九年级下学期第一次联考化学试卷 题型:填空题
如图所示是医院常用的药瓶和注射器,请你据图回答:
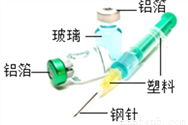
(1)含有金属材料的是___________(写一种即可,下同)
(2)注射器洗净后可以用于家庭小实验,可以代替 __________仪器使用。
(3)钢针一般用不锈钢制造,不容易生锈,钢和生铁的区别是含________量不同。
(4)铁的金属活性比铜强,请写出铁放入硫酸铜溶液中反应的化学方程式: __________。
铝箔或钢针 滴管或量筒 碳 Fe+CuSO4=Cu+FeSO4 【解析】(1)铝箔和钢针是金属材料; (2))注射器可以用于家庭中的滴管或量筒; (3)钢和生铁的区别是含碳量不同; (4)铁与硫酸铜反应生成铜和硫酸亚铁,反应方程式为Fe+CuSO4=Cu+FeSO4;查看答案和解析>>
科目: 来源:安徽省南陵县2018届九年级下学期第一次联考化学试卷 题型:选择填充题
从“丝绸之路”到“一带一路”的倡议,促进了东西方经济、文化的交流。
(1)“丝绸之路”把中国的丝绸、茶叶等传入西方,将西方的宝石等带入中国。丝绸裁剪缝制的过程是_______(选填“物理”或“化学”)变化;新鲜茶叶中含维生素C,其化学式是C6H8O6,维生素C由_______种元素组成;宝石的成分复杂,其中所含的Al2O3属于_______(选填“单质”或“化合物”)
(2)能源合作是“一带一路”的重要内容,中缅油气管道将石油和天然气输入中国。石油是由多种化合物组成的 ______(选填“混合物”或“纯净物”);天然气的主要成分是甲烷(化学式是CH4)请写出甲烷燃烧的化学方程式 _____________________________。
物理 三 化合物 混合物 CH4+2O2点燃2H2O+CO2 【解析】(1)丝绸裁剪缝制的过程中没有新物质的生成,是物理变化;维生素C由碳元素、氢元素、氧元素组成,故共由三种元素组成;Al2O3是由两种元素组成的化合物; (2)石油是由多种化合物组成的混合物;甲烷与空气中的氧气反应生成二氧化碳和水,反应方程式为CH4+2O2点燃2H2O+CO2查看答案和解析>>
科目: 来源:安徽省南陵县2018届九年级下学期第一次联考化学试卷 题型:实验题
正确选择实验仪器是实验成功的重要保证,下面是实验室中常见的仪器,请按要求填空。
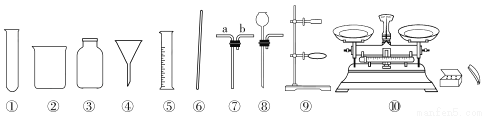
(1)配制一定溶质质量分数的氯化钠溶液,需用到的仪器有______(填序号),还缺少的两种仪器是_______(填名称);过滤粗盐水所用到的仪器有_______(填序号)。
(2)实验室用锌粒和稀硫酸制取氢气,可选上述仪器中的③与⑧组合成发生装置,该反应的化学方程式为______________________________。
(3)利用仪器③与⑦可组合成一个贮气装置,收集氢气(氢气难溶于水、密度小于空气)时,气体应从仪器⑦的________(填“a”或“b”)端通入。该装置还有其他的用途,请你任举一例:________________ 。
②⑤⑥⑩ 药匙和滴管 ②④⑥ Zn+H2SO4=ZnSO4+H2↑ b 装满水用排水法收集气体(其他合理答案均可) 【解析】(1)配制一定溶质质量分数的氯化钠溶液,需用到的仪器有烧杯、量筒、玻璃棒、天平,故选②⑤⑥⑩;其中还缺少药匙和滴管;过滤粗盐水所用到的仪器有烧杯、漏斗、玻璃棒; (2)锌与稀硫酸反应生成硫酸锌和氢气,反应方程式为Zn+H2SO4=ZnSO4+H2↑ ; (3...查看答案和解析>>
科目: 来源:安徽省南陵县2018届九年级下学期第一次联考化学试卷 题型:简答题
A、B、C三种固体物质的溶解度曲线如下图所示。据图回答问题:
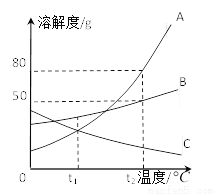
(1)温度为_______ 时,A与C物质的溶解度相等;
时,A与C物质的溶解度相等;
(2)将t1 时A、B、C三种物质的饱和溶液升温到t2
时A、B、C三种物质的饱和溶液升温到t2 有晶体析出的是 ________(填字母代号);
有晶体析出的是 ________(填字母代号);
(3)t2 时,把A、B物质各50g分别加到100g水中,不能形成饱和溶液的是 _______(填字母代号),若要使之达到饱和状态,还需要向溶液中加入____g该溶质,此时该饱和溶液的溶质质量分数为 ______。 图中_______物质的溶解度曲线与气体物质溶解度曲线受温度影响变化相似。
时,把A、B物质各50g分别加到100g水中,不能形成饱和溶液的是 _______(填字母代号),若要使之达到饱和状态,还需要向溶液中加入____g该溶质,此时该饱和溶液的溶质质量分数为 ______。 图中_______物质的溶解度曲线与气体物质溶解度曲线受温度影响变化相似。
查看答案和解析>>
科目: 来源:安徽省南陵县2018届九年级下学期第一次联考化学试卷 题型:科学探究题
铝合金是工业中应用最广泛的一类有色金属结构材料,在航空、航天、汽车、机械制造、 船舶及化学工业中已大量应用。工业经济的飞速发展,对铝合金的需求日益增多,使铝合金的研究也随之深入。已知某铝合金粉末除铝外,还含有铁、铜中的一种或两种。某兴趣小组在老师的指导下,对铝合金粉末中铁、铜的存在情况进行了探究。
【查阅资料】铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水); Fe、Cu不与氢氧化钠溶液反应。
猜想1:该合金粉末中除铝外,还含有铁。
猜想2:该合金粉末中除铝外,还含有铜。
猜想3:该合金粉末中除铝外,还含有铁、铜。
【实验探究】下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液。
实验方案 | 实现现象 | 结论 |
①取一定量的合金粉末,加过量的___________,充分反应后过滤,滤渣备用。 | 粉末部分溶解,并有气体放出。 | 合金中一定含有________ 。 |
②取步骤①所得滤渣,加过量的___________,充分反应。 | 滤渣部分溶解,并有气体放出,溶液呈浅绿色。 | 合金中一定含有_________ 。 |

【探究结论】猜想 _________成立。
【反思】一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质。写出铝与稀盐酸反应的化学方程式 ___________________。
【拓展与分析】
为了验证铝、铁的金属活动性强弱,小刘同学设计了如下实验方案:把表面积相同的铝丝和铁片同时投入到相同体积的稀盐酸中,比较反应的剧烈程度。请你评价该方案在操作过程中和控制变量上的不足之处。
操作过程中的不足之处___________________。
控制变量上的不足之处________________________。
请你再设计一种不同类型的实验方案,验证铝、铁的金属活动性强弱。________________。
略 略 略 略 3 2Al+6HCl=2AlCl3+3H2↑ 操作过程中难以控制铝丝和铁片的表面积相同 没有控制稀盐酸的溶质质量分数相同 将铝丝插入硫酸亚铁溶液中,观察现象。(其他合理答案均可) 【解析】(1) Fe、Cu不与氢氧化钠溶液反应,而铝可以与氢氧化钠反应生成氢气,故应加入过量的氢氧化钠,当看到粉末部分溶解,并有气体放出,说明固体中一定有铝; 滤渣部分溶解,并有气体放出,溶液...查看答案和解析>>
科目: 来源:安徽省南陵县2018届九年级下学期第一次联考化学试卷 题型:计算题
用图1所示装置制取氢气并测定稀硫酸中溶质的质量分数,将稀硫酸全部加入锥形瓶中,天平示数的变化如图2所示,请计算:
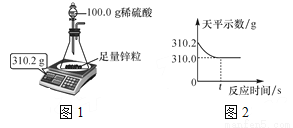
(1)共制取氢气________g;
(2)稀硫酸中溶质的质量分数是_______。
0.2 9.8% 【解析】【解析】 (1) 根据质量守恒定律可得,生成的氢气的质量为310.2 g-310.0 g=0.2 g; (2)由于金属是足量的,所以酸应该是完全反应 设稀硫酸中溶质的质量为x。 Zn+H2SO4=ZnSO4+H2↑ 98 2 x 0.2 g x=9.8 g 稀硫酸中溶质的质量分数为 ×100%=9.8% 答:稀硫酸中...查看答案和解析>>
科目: 来源:洋思中学2018年春学期九年级教学情况化学试卷 题型:单选题
下列变化过程中,发生物理变化的是
A. 葡萄酿酒 B. 干冰升华 C. 苹果腐烂 D. 蛋清受热凝固
B 【解析】A、葡萄酿酒的过程中有新物质的生成,是化学变化,错误; B、干冰升华是固态的二氧化碳变为气态的二氧化碳吸收热量,该过程中没有新物质的生成,是物理变化,正确; C、苹果腐烂是苹果在空气中发现缓慢氧化的过程,是化学变化,错误; D、蛋清受热凝固发生了化学变化,错误。故选B。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com