
科目: 来源:江苏省常州市部分学校2018年九年级中考模拟试卷1 题型:单选题
分离、提纯是化学实验的重要环节,下列实验设计不能达到实验目的是( )
选项 | 实验目的 | 实验设计 |
A | 除去铜粉中混有的少量铁粉 | 用磁铁吸引 |
B | 除去NaCl固体中的少量NaOH | 先加足量水溶解,再加适量稀盐酸,蒸发结晶 |
C | 除去KNO3溶液中的少量K2SO4 | 加入适量的Ba(NO3)2溶液,过滤 |
D | 除去CO中的少量H2O和CO2 | 先通过浓酸,再通过氢氧化钠溶液 |
A. A B. B C. C D. D
D 【解析】A、磁铁可以吸引铁,而不能吸引铜,故可以除去铜粉中的少量的铁,正确; B、氯化钠和氢氧化钠溶液水后,氢氧化钠和稀盐酸反应生成氯化钠,故蒸发后可以获得纯净的氯化钠,正确; C、硝酸钾不与硝酸钡反应,氯酸钾可以与硝酸钡反应,生成硫酸钡沉淀和硝酸钾,正确; D、混合气体先通过浓硫酸后再通过氢氧化钠溶液后又有水带出,错误。故选D。查看答案和解析>>
科目: 来源:江苏省常州市部分学校2018年九年级中考模拟试卷1 题型:单选题
向含有FeSO4和CuSO4的溶液中加入一定质量的Zn粉,充分反应后过滤,向滤渣中加入稀硫酸,有气泡产生,根据上述现象,得出的结论正确的是( )
A. 滤渣中只有Cu B. 滤渣中一定有Fe
C. 滤渣中中一定有Zn D. 滤渣中中一定有Cu、Fe、Zn
B 【解析】A、向滤渣中加入稀硫酸,有气泡产生,说明滤渣中还含有锌或铁,错误; B、锌比铁活泼,当锌过量时,滤渣中有铜、铁、和锌,当锌不足时,滤渣中有铁和铜,正确; C、当锌不足不能将铁置换完,则滤渣中没有新,错误; D、由题可知,滤渣中一定有铁和铜,错误。故选B。查看答案和解析>>
科目: 来源:江苏省常州市部分学校2018年九年级中考模拟试卷1 题型:单选题
将一定质量的铁和氧化铜的混合物粉末放入足量量稀盐酸中,充分反应后产生气体0.4g,井得到残留固体6.4g。则原混合物粉末的质量是( )
A. 8.0g B. 11.2g C. 16.0g D. 24.8g
D 【解析】将一定质量的铁和氧化铜的混合物粉末放入足量量稀盐酸中,氧化铜先和稀盐酸反应生成氯化铁和水,铁和稀盐酸反应生成氯化亚铁和氢气,铁与氯化铜反应生成铜,最终生成铜的质量为6.4g,故氧化铜的质量为6.4g=8g;铁与盐酸反应生成氢气的关系式是 Fe—H2,设生成0.4g的氢气需要铁的质量为x, Fe—H2 56 2 x 0.4g =,x=11.2g, ...查看答案和解析>>
科目: 来源:江苏省常州市部分学校2018年九年级中考模拟试卷1 题型:单选题
将一定质量的Ba(OH)2溶液与Na2CO3溶液混合恰好完全反应,向反应后的混合物中加入稀盐酸,产生气体的体积与加入稀盐酸的体积的关系如图所示,下列说法中正确的是
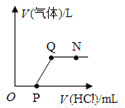
A. N点时,所得溶液的pH=7
B. Q点时,所得溶液中的溶质只含有BaCl2
C. O至P段发生反应的化学方程式为NaOH+HCl=NaCl+H2O
D. P至Q段发生反应的化学方程式为Ba(OH)2+2HCl=BaCl2+2H2O
C 【解析】试题分析:从图示看:原来的反应物中二者恰好反应会生成氢氧化钠和碳酸钡,所以开始加入盐酸后没有立即产生气体,而是盐酸先和氢氧化钠反应,O至P段发生反应的化学方程式为NaOH+HCl=NaCl+H2O;当Q点后碳酸钡和氢氧化钡都恰好反应完,P至Q段发生反应的化学方程式为BaCO3+2HCl=BaCl2+H2O+CO2↑;Q点时,所得溶液中的溶质只含有BaCl2和NaCl;所以此时的P...查看答案和解析>>
科目: 来源:江苏省常州市部分学校2018年九年级中考模拟试卷1 题型:填空题
化学用语是化学学习的重要工具。写出下列化学用语:
(1)2个甲烷分子_________;(2)3个铝离子_________;(3)2个最小的原子_________; (4)氧化铁中铁元素的化合价_________。
2CH4 3Al3+ 2H +3 【解析】(1)1个甲烷分子中含有1个碳原子和4个氢原子,表示为CH4,2个甲烷分子是在甲烷的化学式的前面加上2 ,表示为2CH4; (2)离子是在元素符号的右上角用数字加上正负号来表示,若要表示多个离子,在离子符号的前面加上数字,3个铝离子表示为3Al3+; (3)最小的原子是氢原子,2个氢原子表示为2H ; (4)氧化铁中氧元素的化合价为...查看答案和解析>>
科目: 来源:江苏省常州市部分学校2018年九年级中考模拟试卷1 题型:选择填充题
化学就在我们身边。请从下列物质中,选择适当的字母填空。
A.稀盐酸;B.氢气;C.武德合金;D.液态空气;E.硫酸铜。
(1)常用于去除铁锈的是_________;(2)常用于工业上制取氧气的是_________;(3)常用于游泳池消毒杀菌的是_________;(4)常用作清洁能源的是_________;(5)常用作保险丝的是_________。
A D E B C 【解析】(1)常用稀盐酸除去铁锈,故选A; (2)工业上用液态的空气制取氧气,故选D; (3)游泳池常用硫酸铜来杀菌消毒,故选E ; (4)氢气是最清洁的能源,故选B; (5)武德合金的熔点低,可以做保险丝,故选C;查看答案和解析>>
科目: 来源:江苏省常州市部分学校2018年九年级中考模拟试卷1 题型:填空题
A、B、C三种物质质的溶解度曲线如图所示。请回答下列问题:
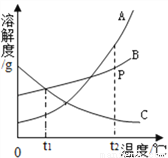
(1)P点对应的是物质A的_________(“饱和”或“不饱和”)溶液;
(2)加热C的饱和溶液,出现浑浊现象,其原因是_______________________;
(3)除去B中少量的A,步骤是:溶解→蒸发结晶→_________→洗涤干燥。
(4)将t2℃的这三种物质的饱和溶液分别降温至t1℃,所得的溶液中溶质的质量分数分别是ω(A)、ω(B)和ω(C),则三者的大小关系是___________________。
不饱和 C物质的溶解度随温度的升高而降低,升高温度C的饱和溶液析出C 趁热过滤 ω(B)>ω(A)>ω(C) 【解析】(1)P点在A物质的溶解度曲线的下方,故P点对应的是物质A的不饱和溶液; (2)C物质的溶解度随温度的升高而降低,故升高温度C的饱和溶液析出C; (3)A物质的溶解度随温度的升高而升高,变化较大,B物质的溶解度随温度的升高而升高,变化不大,故除去B中少量的A,步骤...查看答案和解析>>
科目: 来源:江苏省常州市部分学校2018年九年级中考模拟试卷1 题型:实验题
化学实验是进行科学探究的重要手段。
(1)黄铜是铜锌合金,将外形完全相同的纯铜片和黄铜片相互刻划,该实验的目的是比较它们的_____________大小。
(2)用坩埚钳夹取一小块木炭,在酒精灯上加热至燃烧,然后将木炭插入盛有氧气的集气瓶内,观察现象。据此可知,可燃物燃烧的剧烈程度与_________________有关。
(3)用图A所示的装置可测定空气中氧气的含量。该实验的原理是通过____________(选填“化学”或“物理”)方法分离或除尽混合物中的某组分,从而测定混合物中该组分的含量。
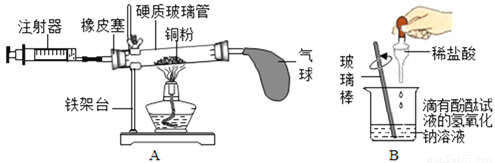
(4)用图B所示的装置探究酸碱中和反应。将稀盐酸滴入滴有酚酞试液的氢氧化钠溶液至过量,观察到的现象是_________________。从微观角度分析,该反应的实质是__________________。请另外写出一个符合上述反应实质的化学方程式______________。
硬度 氧气浓度 化学 红色消失 H+和OH—结合成H2O 2NaOH+H2SO4=Na2SO4+2H2O 【解析】(1)刻划后纯铜的表面有痕迹,故该实验的目的是比较铜和铜合金的硬度大小; (2)木炭在空气中燃烧放出红光,在氧气中燃烧比空气中更剧烈,发出白光,不燃烧的结论程度与氧气的浓度有关; (3)该实验的原理是利用铜与空气中的氧气反应耗掉空气中的氧气,故是化学方法; (4...查看答案和解析>>
科目: 来源:江苏省常州市部分学校2018年九年级中考模拟试卷1 题型:实验题
化学是一门以实验为基础的学科。请结合下列实验装置回答问题。
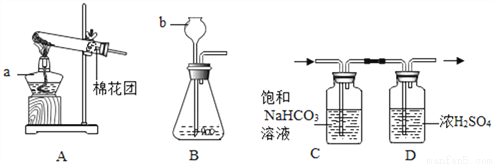
(1)写出图中所示实验仪器的名称:b_______________________________;
(2)写出A装置制取氧气反应的化学方程式______________________________;
(3)检查装置B气密性良好的方法和现象是____________________________,用此装置制得的CO2常含杂质,李静同学利用上图C、D装置除去杂质,得到纯净、干燥的CO2气体,C中足量饱和 NaHCO3溶液的作用是____________________________;
(4)实验室取13.6g溶质质量分数为5%的过氧化氢溶液,充分分解后,可以得到氧气_______克?
长颈漏斗 2KMnO4==== KMnO4+MnO2+ O2↑ 向长颈漏斗加水形成液封,将导管放入水中,双手紧贴锥形瓶外壁,若导管口有气泡产生,移开双手,导管内形成一段稳定的水柱,装置不漏气 除尽氯化氢气体 0.32g 【解析】(1)b仪器的名称是长颈漏斗; (2)A装置是高锰酸钾在加热的条件下反应生成锰酸钾、二氧化锰和氧气,反应方程式为2KMnO4△ KMnO4+MnO2+ O2↑;...查看答案和解析>>
科目: 来源:江苏省常州市部分学校2018年九年级中考模拟试卷1 题型:科学探究题
实验与探究是化学学习的重要方法和内容,李明看到家里多年未用的铜制火锅上有绿色的锈迹,他对绿色锈迹的成分和性质产生了浓厚兴趣。
【查阅资料】
(1)碱石灰是CaO和NaOH的固体混合物;(2)铜表面绿色锈迹的主要成分为碱式酸铜。
【发现问题】
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色液滴生成。为了进一步确定碱式碳酸铜受热分解的产物,进行了如下探究:
探究一:碱式碳酸铜受热分解生成的黑色固体成分。
【猜想与假设】该黑色固体可能是①碳粉;②氧化铜;③_______________________________。
【设计方案】请帮助该同学完成下述实验报告:
实验操作与现象 | 实验结论 |
___________________ | 猜想②正确 |
探究二:碱式碳酸铜受热分解还会生成CO2和H2O。
【进行实验】选择如下图所示装置进行验证
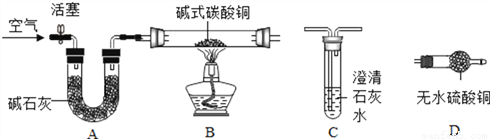
步骤一:连接A和B,打开活塞,通入一段时间的空气;
步骤二:点燃酒酒精灯,依次连接装置A→B→________→_______(填“C”,“D”);
步骤三:点燃酒精灯,观察到明显现象后,停止加热。
【解释与结论】
①当观察到_________________________________,说明碱式碳酸铜受热分解生成了H2O,写出装置C中反应的化学方程式________________________;
②写出Cu2(OH)2CO3受热分解的化学方程式___________________;
【反思与评价】
上述装置中A的作用是________________________。
炭粉和氧化铜 取少量样品于试管中,加入足量稀硫酸,若固体全部溶解,溶液变为蓝色 D C D中固体变蓝 CO2+Ca(OH)2=CaCO3↓+H2O Cu2(OH)2CO3=2CuO+H2O+CO2 ↑ 除尽空气中的二氧化碳和水 【解析】(1)该黑色固体可能是碳粉盒氧化铜的混合物; (2)氧化铜可以与酸反应生成蓝色的溶液,而碳不与酸反应,故可以取少量样品于试管中,加入足量稀硫酸,若固体全...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com