
科目: 来源:江苏省2018届九年级下学期期中考试化学试卷 题型:实验题
请结合下列实验常用装置,回答有关问题。

(1)写出仪器a的名称__________。
(2)实验室用氯酸钾和二氧化锰制取氧气,可采用的发生装置为_______,发生反应的化学方程式是__________。若改用高锰酸钾制取氧气,发生装置应作的改动是_________。
(3)实验室制取二氧化碳的化学方程式为__________________________,若要制取一瓶二氧化碳,可采用的装置组合为_________,向集气瓶中倒入澄清石灰水,发现澄清石灰水溶液不变浑浊,造成这一现象的可能原因是____________________,若要使反应停止可采取的操作是__________________________。
(4)焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:采用下图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置I中产生气体的化学方程式为:H2SO4(浓)+Na2SO3═Na2SO4+SO2↑+H2O

①装置Ⅱ中生成Na2S2O5晶体发生的是化合反应,其反应的化学方程式为:____________。
②Na2S2O5中硫元素的化合价是_____________ 。
③装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为___________ (填序号)。

查看答案和解析>>
科目: 来源:江苏省2018届九年级下学期期中考试化学试卷 题型:流程题
氧化铜矿石含有CuO、Cu2(OH)2CO3和Fe2O3,还含有一些不溶于水、不溶于酸的其他杂质。铜、铁是畜禽所必需的微量元素,某饲料厂联合生产硫酸铜晶体和硫酸亚铁晶体的主要工艺流程如下。

【资料】Cu2+、Fe3+以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Cu(OH)2 |
开始沉淀的pH | 1.5 | 4.2 |
沉淀完全的pH | 3.7 | 6.7 |
请回答问题:
(1)氧化铜矿石粉碎的目的是________________________________。
(2)写出“酸浸”中发生反应的化学方程式__________________(任写一个)。
(3)该流程中氢氧化铁能与硫酸反应,其基本反应类型是_________反应。
(4)下图为“硫酸亚铁干燥曲线图”,据此可确定由FeSO4·7H2O脱水得到流程中所示产品的适宜工艺条件为__________________(填写温度和时间)。

(5)在“调节pH/过滤”中,加入CaCO3调节溶液的pH,请说出溶液适宜的pH范围是____________。
增大接触面积,加快充分反应 Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑ 复分解 125℃(±5) 4h 3.7-4.2 【解析】(1)根据反应物的接触面积与反应速率成正比进行分析;(2)根据碱式碳酸铜和稀硫酸反应会生成硫酸铜、水和二氧化碳进行分析;(3)根据酸碱中和属于复分解反应解答;(4)根据流程图及“硫酸亚铁干燥曲线图”分析解答;(5)根据表中以氢氧化物形式沉...查看答案和解析>>
科目: 来源:江苏省2018届九年级下学期期中考试化学试卷 题型:科学探究题
同学们对制作糕点常用膨松剂Na2CO3或NaHCO3进行了下列探究。
【查阅资料】
溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |

【探究一】NaHCO3和Na2CO3性质差异的探究
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显_____色;酸碱度:NaHCO3溶液________Na2CO3溶液(填“>”或”“<”)。
(2)稳定性:按下图,实验中可观察乙烧杯中的石灰水变浑浊,甲烧杯不变,则乙烧杯中发生反应的化学方程式为:___________________________。结论:在受热条件下,碳酸钠比碳酸氢钠稳定性______(填“强”或“弱”)。

(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的_______。(选填A、B或C)
A.1.5g B.0.96g C.0.5g
【探究二】测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(下图,夹持装置略)

【问题讨论】
(4)实验前先通一段时间的空气的目的是____________________;
(5)A的作用是_____________________________,若没有装置E,NaHCO3的质量分数测定结果会_____________(填“偏大”、“不变”或“偏小”)。
(6)停止加热后,仍继续通入空气一段时间,目的是___________________。
【含量测定】
(7)测得装置D的质量实验前为120.2g,实验后为122.4g,计算该样品中NaHCO3的质量分数。(要有计算过程)______________________
【知识拓展】
(8)向饱和的氯化钠溶液中通入氨气和二氧化碳,经过一系列变化,也可制得Na2CO3和一种铵盐。该反应的化学反应方程式为:_______________________。
蓝 < CO2+Ca(OH)2═CaCO3↓+H2O 强 A 排尽原装置中的空气,防止二氧化碳干扰实验 除去空气中的二氧化碳 偏大 使反应生成的二氧化碳全部被D吸收 84% 2NaCl+H2O+2NH3+CO2=Na2CO3+2NH4Cl 【解析】【探究一】(1)根据溶液pH值分析酸碱性解答;据测定溶液酸碱度的方法以及溶液的酸碱度与酸碱性的关系来分析;(2)根据碳酸氢钠加热分解为碳酸钠、水和...查看答案和解析>>
科目: 来源:云南民族大学附属中学2018届九年级下学期第二次月考化学试卷 题型:单选题
下列说法中正确的是( )
A. 红磷在氧气中能燃烧,在空气中不能燃烧
B. 硫在氧气中燃烧后生成有刺激性气味的气体
C. 镁条在氧气中燃烧时,火星四射,生成黑色固体
D. 木炭伸入盛有氧气的集气瓶中剧烈燃烧,发出白光
B 【解析】A、红磷在氧气中燃烧,在空气中也能燃烧,错误;B、硫在氧气中燃烧,产生一种具有刺激性气味的气体,正确;C、镁条在氧气中燃烧,发出耀眼的白光,生成一种白色固体,错误;D、木炭伸入盛有氧气的集气瓶中,若不点燃,不会剧烈燃烧,错误。故选B。查看答案和解析>>
科目: 来源:云南民族大学附属中学2018届九年级下学期第二次月考化学试卷 题型:单选题
 常用于在接触法制硫酸过程中产生
常用于在接触法制硫酸过程中产生 ,其化学方程式为:4FeS2 +11O2
,其化学方程式为:4FeS2 +11O2  2X+8SO2,则X的化学式为
2X+8SO2,则X的化学式为
A. FeO B.  C.
C.  D.
D. 
查看答案和解析>>
科目: 来源:云南民族大学附属中学2018届九年级下学期第二次月考化学试卷 题型:单选题
下列实验设计或结论合理的是
A. 向某固体滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐
B. 除去 溶液中混有的少量
溶液中混有的少量 ,可加入适量的
,可加入适量的 ,充分搅拌后过滤
,充分搅拌后过滤
C.  、
、 、
、 、
、 四种离子可在
四种离子可在
D. 将带火星的木条伸入到装有气体的集气瓶中,木条不复燃,证明该气体中不含氧气
C 【解析】A、向某固体滴加稀盐酸,有气泡产生,则该固体不一定是碳酸盐,活泼金属与稀盐酸也可以产生气体,故A错误;B、除去MgCl2溶液中混有的少量CuCl2,不可加入适量的Mg﹙OH﹚2,氢氧化镁不溶于水,与氯化铜不反应,故B错误;C、pH=12,溶液呈碱性,CO32-,Na+,NO3-,K+四种离子与OH- 离子均不反应,可以大量共存,故C正确; D、将带火星的木条伸入到装有气体的集气瓶...查看答案和解析>>
科目: 来源:云南民族大学附属中学2018届九年级下学期第二次月考化学试卷 题型:单选题
“超临界水”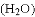 因具有许多优良特性而被科学家追捧,它是指当温度和压强达到一定值时,水的液态和气态完全交融在一起的状态,用“
因具有许多优良特性而被科学家追捧,它是指当温度和压强达到一定值时,水的液态和气态完全交融在一起的状态,用“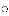
 ”表示氧原子,下列模型能表示“超临界水”分子的是
”表示氧原子,下列模型能表示“超临界水”分子的是
A.  B.
B.  C.
C.  D.
D. 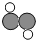
查看答案和解析>>
科目: 来源:云南民族大学附属中学2018届九年级下学期第二次月考化学试卷 题型:单选题
下列各项中,属于我国


A.  浓度 B.
浓度 B.  浓度 C.
浓度 C.  浓度 D.
浓度 D.  浓度
浓度
查看答案和解析>>
科目: 来源:云南民族大学附属中学2018届九年级下学期第二次月考化学试卷 题型:单选题
把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质量如表所示:
物 质 | A | B | C | D |
反应前质量 |
|
|
|
|
反应后质量 | 待测 |
| 0 |
|
下列说法正确的是
A. 物质C一定是反应物,物质D可能是单质
B. 反应后密闭容器中A的质量为
C. 反应过程中,物质B和物质D变化的质量比为87:36
D. 若物质A与物质C的相对分子质量之比为194:216,则反应中A和C的化学计量数之比为2:1
A 【解析】根据质量守恒定律知,A+C→B+D。A、物质C一定是反应物,物质D可能是单质,故A正确;B、反应后密闭容器中A的质量为19.7-﹙8.7+3.2-21.6﹚=10,故B错误;C、反应过程中,物质B和物质D变化的质量比为8.7∶3.2,故C错误;D、若物质A与物质C的相对分子质量之比为194:216,则反应中A和C的化学计量数之比为XA∶YC=9.7∶121.6,X∶Y=1∶2,故...查看答案和解析>>
科目: 来源:云南民族大学附属中学2018届九年级下学期第二次月考化学试卷 题型:单选题
除去下列物质中混有的杂质,所用试剂和操作方法不正确的是
物质 | 所含杂质 | 除杂质选用的试剂或方法 | |
A | NaCl溶液 | NaOH | 滴加适量的稀盐酸 |
B | Cu | Fe | 加入足量的稀盐酸并过滤 |
C |
| CO | 在氧气中点燃 |
D |
|
| 加入足量的水溶解并过滤、洗涤、干燥 |
A. A B. B C. C D. D
C 【解析】 物质 所含杂质 除杂质选用的试剂或方法 A NaCl溶液 NaOH 滴加适量的稀盐酸,遇氢氧化钠反应生成氯化钠和水,故A正确; B Cu Fe 加入足量的稀盐酸,遇铁反应生成氯化亚铁,与铜不反应,过滤,故B正确; C CO 在氧气中点燃,一氧化碳量很少,很难通过点燃除去,二氧化碳中混有...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com