
科目: 来源:江苏省常州市2018届九年级下学期期中考试化学试卷 题型:单选题
某工厂原来用氢氧化钠溶液中和所排废水中的硫酸,现改用氢氧化钾溶液中和以得到钾肥。若氢氧化钾溶液的溶质质量分数与原来所用氢氧化钠溶液的溶质质量分数相同,则此时碱流量阀应如何调节
A. 加大流量 B. 减小流量 C. 无需变动 D. 无法确定
A 【解析】都发生反应OH-+H+═H2O,两种碱溶液的密度基本相同,根据c=可知,质量分数相同,KOH的物质的量浓度减小,若流量不变,相同体积内KOH的物质的量减少,不能将废水的硫酸中和,故应该将流量阀开大一些才能中和掉定量的硫酸,故选A。查看答案和解析>>
科目: 来源:江苏省常州市2018届九年级下学期期中考试化学试卷 题型:综合题
⑴ 按要求写化学用语:
纯碱________;二氧化硫分子_______;两个硝酸根离子_______;
⑵ 判断下列物质的类别,并用相应的序号填空
① 单质 ② 氧化物 ③ 酸 ④ 碱 ⑤ 盐
物质化学式 | Fe2O3 | CuSO4 | Ca(OH)2 |
物质类别 | ________ | _______ | _______ |
查看答案和解析>>
科目: 来源:江苏省常州市2018届九年级下学期期中考试化学试卷 题型:综合题
⑴ 请从下列物质中选择适当的物质填空(填序号):
A.干冰 B.盐酸 C.明矾 D.生石灰 E.葡萄糖
①能被人体直接吸收的营养物质是________; ②可用于人工降雨的物质是________; ③可用于净水的物质是________; ④常用作袋装食品的干燥剂________。
⑵ 根据题意用下列选项的字母填空:A.熔点 B.沸点 C.硬度
①工业制氧气和石油分馏都是利用混合物中各成分的________不同;
②武德合金用作保险丝比用纯铜丝更安全,是因为前者的________低。
E A C D B A 【解析】(1) ①能被人体直接吸收的营养物质是葡萄糖;②干冰升华吸热,可用于人工降雨;③可用于净水的物质是明矾;④常用作装食品的干燥剂生石灰;(2)①工业制氧气和工业石油分馏都是利用混合物中各成分的沸点不同;②武德合金用作保险丝比用纯铜丝更安全,是因为前者的熔点低。查看答案和解析>>
科目: 来源:江苏省常州市2018届九年级下学期期中考试化学试卷 题型:综合题
(1)人类使用的化石燃料主要是煤、石油和________________,直接燃煤会形成严重的酸雨,酸雨是指pH小于______________的降水;
(2)为减少温室气体二氧化碳的排放,可以将二氧化碳进行转化。下图为该反应的微观示意图,根据图示回答下列问题:
反应前 | 反应后 |
| |
A | B | C | D |
|
|
|
|
①以上4种物质中属于有机化合物的是________________(填化学式);
②在反应中C与D质量比为____________________;
(3)氢能是理想的清洁能源。以太阳能为热源,经由铁氧化合物循环分解水的过程如图:
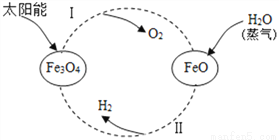
①反应Ⅰ的基本反应类型为___________________;
②写出在一定条件下发生的反应的Ⅱ化学方程式:_____________;
③在上述循环过程中,最终得到的产品是________。
天然气 5.6 CH4 9:4 分解反应 3FeO+H2O=Fe3O4+H2↑ H2、O2 【解析】(1)人类使用的化石燃料主要是煤、石油和天然气,直接燃煤会形成严重的酸雨,酸雨是指pH小于5.6的降水;(2)由反应的微观示意图可知,CO2+4H22H2O+CH4,①以上4种物质中属于有机化合物的是CH4;②在反应CO2+4H22H2O+CH4中 36 16 C与D质量比为:36...查看答案和解析>>
科目: 来源:江苏省常州市2018届九年级下学期期中考试化学试卷 题型:计算题
火力发电厂用石灰石浆吸收废气中的二氧化硫,以防止污染环境,方程式为2CaCO3+2SO2+O2==2CaSO4+CO2。我市某火电厂每日消耗动力煤10000t同时产生二氧化硫气体192t,则理论上至少需要含碳酸钙为80%的石灰石多少吨?
375t 【解析】根据产生的二氧化硫全部被碳酸钙吸收,设需含CaCO380%的石灰石的质量为x,则含纯物质CaCO3的质量为80%×x, 2CaCO3+2SO2+O2═2CaSO4+2CO2 200 128 80%×x192t ,解得:x=375t。 答:理论上至少需要含碳酸钙为80%的石灰石375吨。查看答案和解析>>
科目: 来源:江苏省常州市2018届九年级下学期期中考试化学试卷 题型:实验题
实验室用如图所示装置制取并收集气体
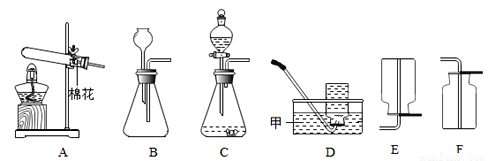
请回答下列各题
⑴ 仪器甲的名称________;
⑵用A装置制取氧气,则反应的化学方程式是___________;
⑶能直接用于实验室制取氢气的发生装置有________(填序号),能用于收集氢气的装置是_____________(填序号);
⑷下图为家庭制氧机内桶构造示意图,桶上设有制氧剂投药口和出气口。制氧时,在桶内Ⅰ、Ⅱ两室中装入一定量的水,而后从投药口中投入药品后,并立即将其关闭,从出气口即可呼吸氧气。
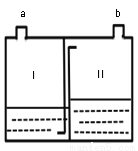
已知:i.制氧剂的主要成分是过碳酸钠和催化剂,过碳酸钠在水中能分解产生过氧化氢;
ii.产生的氧气需通入水中净化。
① 制氧机中过氧化氢发生反应的化学方程式为_________________;
② 氧气的出口为_________(填“a”或“b”)。
水槽 2KMnO4K2MnO4+MnO2+O2↑ C DE 2H2O22H2O+O2↑ a 【解析】⑴ 仪器甲的名称水槽;⑵用A装置制取氧气,属于固固加热型,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是:2KMnO4K2MnO4+MnO2+O2↑;(3)实验室和用锌稀硫酸反应制取氢气,属于固液不加热型,故发生装置选C,B装置导管伸入过长,错误;氢气,难溶于水,可用排水...查看答案和解析>>
科目: 来源:江苏省常州市2018届九年级下学期期中考试化学试卷 题型:科学探究题
某兴趣小组用图1装置进行实验时发现:烧杯中饱和石灰水先变浑浊,后逐渐澄清。
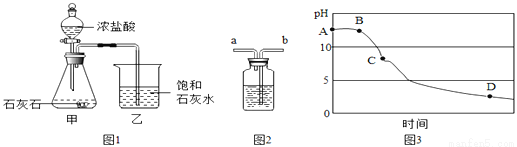
⑴ 写出甲装置中发生反应的化学方程式_______________;
⑵ 为探究“饱和石灰水浑浊后变澄清的原因”,该小组同学开展了如下活动:
【查阅文献】碳酸钙(碳酸钠等)与二氧化碳、水反应生成可溶于水的碳酸氢钙(碳酸氢钠等)
【提出假设】假设1:二氧化碳与碳酸钙、水发生反应生成碳酸氢钙;
假设2:__________________________;
【设计实验】为除去CO2中的氯化氢气体,小华在图1中甲、乙装置之间增加图2装置,装置的连接顺序是甲→_________→_________→乙(填字母序号);其中盛放的试剂合理的是___________(填选项序号:A.浓硫酸 B.NaOH溶液 C.饱和NaHCO3溶液;
【实验现象】饱和石灰水浑浊后,继续通入足量CO2,沉淀部分溶解但最终并未完全澄清。
【得出结论】假设2成立;
⑶同学们在老师指导下仍用图1所示装置进行实验,但同时用pH传感器监测烧杯中溶液的pH,所得图像如图3所示:
①AB段pH几乎不变的原因可能是_____________________;D点处溶液的溶质主要有(填化学式)__________;
② BC段主要发生两个化学反应:a二氧化碳与澄清石灰水反应;b(写出化学方程式)_______________。
CaCO3+2HCl=CaCl2+H2O+CO2↑ 挥发出的HCl气体进入乙烧杯中溶解生成的碳酸钙 b a C 一开始排出来的是空气进入到了乙烧杯中,对pH基本没有影响 CaCl2 和 HCl 2HCl+Ca(OH)2=CaCl2+2H2O 【解析】(1)甲装置中石灰石的主要成分碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑...查看答案和解析>>
科目: 来源:江苏省常州市2018届九年级下学期期中考试化学试卷 题型:科学探究题
订书钉是生活中常用文具,顾老师指导同学们围绕订书们钉开展实验研究。
实验步骤 | 实验内容 |
① | 用磁铁吸引订书钉,发现订书钉能被吸引 |
② | 取一个订书钉块(40根钉子)(如图甲所示),浸入酒精中,一段时间后能从订书钉块上取下一层胶水薄膜 |
③ | 取上述订书钉块用棉花擦去精,并待酒精完全挥发后称量其质量为13.4g |
④ | 将其放入图乙所示装置,并在干管口用氢气传感器测量氢气质量,同时记录质量变化 (如图丙所示) |
⑤ | 5.8分钟时停止反应取出装置剩余订书钉,洗涤、干操、称量,剩余订书钉质量为7.8g |

问题思考:
(1)订书钉表面涂胶水的目的主要是_______________;
(2)查阅资料可知:订书钉主要成分为铁,并在其表面镀一种金属。请结合图丙分析:
①图丙中P点纵坐标X的值_______________________;
②0→0.2分钟不产生氢气的原因主要是______________;
③请写出1.7分钟后装置中发生的主要化学反应方程式____________;
④订书钉表面镀的金属可能是钙、镁、铝、锌、铜中的一种,请根据实验分析该金属是_______。
防止订书钉生锈 0.18g 订书钉表面有少量金属氧化物与酸反应 Fe+H2SO4==FeSO4+H2↑ Zn 【解析】(1)订书钉表面涂胶水的目的主要是防止订书钉生锈;(2) ①根据质量守恒定律,反应图丙中P点纵坐标表示生成氢气的质量,故X=213.4g-213.22g=0.18g;②0→0.2分钟不产生氢气的原因主要是订书钉表面有少量金属氧化物与酸反应;③请写出1.7分钟后铁与硫酸反应生成...查看答案和解析>>
科目: 来源:江苏省常州市2018届九年级下学期期中考试化学试卷 题型:流程题
现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
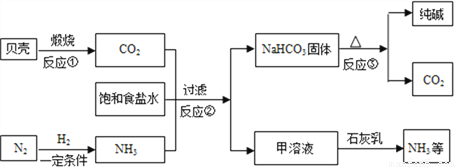
(1)已知20℃,氧化钠溶解度为36g,则20时饱和食盐水溶质质量分数为______________;(保留1位小数)
(2)反应①的化学方程式是_______________________;
(3)甲溶液中能与石灰乳反应生成氨气的物质是_____________,实验室中通常检验氨气的试剂是______________;
(4)反应②的化学方程式是_____________________;
(5)整个生产过程中可循环利用的物质是_________________;
(6)为测定产品纯碱中钠元素质量分数,取样(样品中除纯碱外还含有碳酸氢钠和少量不溶性杂质)设计如下实验过程:
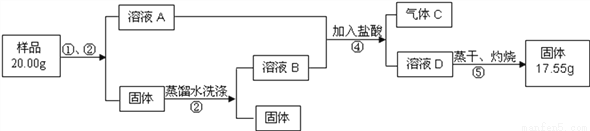
请回答:
Ⅰ.操作①是溶解,操作②为__________________;
Ⅱ.原样品中钠元素的质量分数为___________________;
Ⅲ.若测定结果偏低,原因可能是__________(填字母)。
A.溶液D中含有Na2CO3 B.溶液D中含有NaCl
C.操作③中固体没有洗涤干净 D.操作④中加入过量的盐酸
26.5% CaCO3CaO+CO2↑ NH4Cl 湿润的红色石蕊试纸 NaCl+CO2+ NH3+H2O=NaHCO3,↓+NH4Cl CO2和NH3 过滤 34.5% AC 【解析】(1)已知20℃,氧化钠溶解度为36g,则20时饱和食盐水溶质质量分数为: ;贝壳的主要成分是碳酸钙,碳酸钙在高温的条件下分解生成氧化钙和二氧化碳,化学方程式为:CaCO3CaO+CO2↑;(3)氯化铵和氢氧...查看答案和解析>>
科目: 来源:山东省威海市文登区八校(五四学制)2017-2018学年八年级下学期期中考试化学试卷 题型:单选题
我们身边有很多公关标志,下面与消防安全无关的标志是( )
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com