
科目: 来源:北京市门头沟区2018届九年级一模化学试卷 题型:填空题
生活中的能量大部分来自于化石燃料的燃烧。化石燃料包括煤、________和天然气。天然气燃烧的化学方程式为_____________________。
石油 CH4 + 2O2CO2 + 2H2O 【解析】本题考查了化石燃料的种类、甲烷的燃烧。 煤、石油和天然气是常见的化石燃料,天然气的主要成分是甲烷,甲烷完全燃烧生成二氧化碳和水,反应的化学方程式为:CH4 + 2O2 CO2 + 2H2O。查看答案和解析>>
科目: 来源:北京市门头沟区2018届九年级一模化学试卷 题型:科学探究题
阅读下面科普短文(本文由网络文章改写)。
松花蛋又称皮蛋、变蛋、灰包蛋等,因剥开蛋壳后胶冻状的蛋清中常有松针状的结晶或花纹而得名,是一种我国传统风味食品,口感鲜滑爽口,色香味均有独到之处。中医认为,松花蛋性凉,对牙痛、眼痛等疾病有一定疗效。由于松花蛋会有一股碱涩味,在吃松花蛋的时候可以加入少量的姜醋汁。
松花蛋是用料泥包裹鸭蛋、鸡蛋等加工而成。料泥是由生石灰、纯碱、食盐、红茶、草木灰(主要成分K2CO3)等原料与水按比例混合均匀制得。料泥制作过程中,通过一系列反应,产生的强碱(NaOH、KOH)经蛋壳渗入到蛋清和蛋黄中,与其中的蛋白质作用,致使蛋白质分解、凝固并放出少量硫化氢气体和氨气。同时渗入的碱还会与蛋白质分解出的氨基酸进一步发生中和反应,生成的盐的晶体沉积在凝胶态的蛋清中,便出现了朵朵“松花”。而硫化氢气体则与蛋清和蛋黄中的矿物质作用生成各种硫化物,使蛋清和蛋黄的颜色发生改变,蛋清呈特殊的茶褐色、蛋黄则呈墨绿色。下图表示松花蛋腌制时间与其中蛋清和蛋黄的pH的变化关系。

很多人在平时生活中都非常喜欢吃皮蛋瘦肉粥、凉拌松花蛋,专家提醒这种食物少吃无妨,却不能过多食用。其一,松花蛋腌制过程中蛋白质分解、变质,导致营养价值遭到了一定的破坏。其二,市售松花蛋还可能含铅(国家规定松花蛋中铅含量需小于0.5mg/kg)。微量铅很容易被儿童吸收,导致铅中毒。其三,剥开皮的松花蛋1至2小时内一定要吃完,若长时间暴露在空气中,非常容易感染沙门氏杆菌,沙门氏杆菌会快速繁殖,此时食用松花蛋很容易引起中毒现象,依据文章内容,回答下列问题。
(1)食用松花蛋时加入少量姜醋汁可以除去松花蛋中________味。
(2)料泥制作过程中会生成强碱NaOH和KOH,钾元素来自于原料中的________。请写出Na2CO3与Ca(OH)2反应的化学方程式为________。
(3)依据松花蛋腌制时间与其中蛋清和蛋黄pH的变化关系判断,当蛋清和蛋黄pH均达到9以上时,松花蛋至少腌制的天数为________(填字母序号,下同)。
A.2天 B.6天 C.12天 D.32天
(4)下列关于松花蛋的说法正确的是________。
A.松花蛋特殊颜色的形成与硫化氢气体有关
B.松花蛋具有很高的营养价值,成人可以多吃
C.市售松花蛋可能含有少量的铅,儿童不宜食用
D.剥开皮的松花蛋隔夜放置后依然可以放心食用
碱涩味 草木灰(或K2CO3) Ca(OH)2 + Na2CO3 === CaCO3↓+ 2NaOH B AC 【解析】本题在“松花蛋”的情境下考查盐的化学性质,生石灰的性质与用途,质量守恒定律及其获得信息,处理信息的能力。认真阅读,结合已有的知识进行分析。 (1)姜醋汁呈酸性,可以中和碱水。食用松花蛋时加入少量姜醋汁可以除去松花蛋中碱涩味; (2)料泥制作过程中会生成强碱NaO...查看答案和解析>>
科目: 来源:北京市门头沟区2018届九年级一模化学试卷 题型:综合题
尿素[CO(NH2)2]是一种常用化肥。下图为利用天然气制尿素的主要流程。
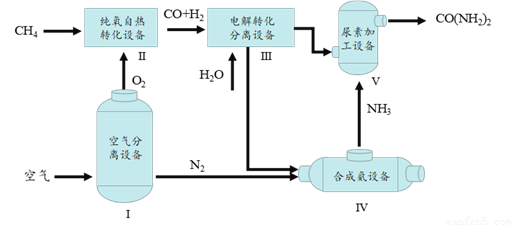
(1)设备Ⅰ内发生的变化是________(填“物理变化”或者“化学变化”)。
(2)设备Ⅱ中发生的反应所属的基本反应类型是_________。
(3)设备Ⅲ中产生并分离出CO2和H2两种物质,依据流程图判断进入设备Ⅳ的是H2,理由是________。
(4)设备Ⅴ中发生反应:2NH3+CO2  CO(NH2)2+H2O,若生产60 t尿素,需要NH3的质量为_______t。
CO(NH2)2+H2O,若生产60 t尿素,需要NH3的质量为_______t。
查看答案和解析>>
科目: 来源:北京市门头沟区2018届九年级一模化学试卷 题型:实验题
请从A或B两题中任选1个作答,若两题均作答,按A计分。
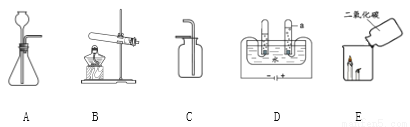
A | B |
(1)实验室用高锰酸钾制取氧气,选取的发生装置是______。 (2)实验室用高锰酸钾制取氧气的化学方程式为___________________。 (3)D中试管a中产生的气为____。 | (1)实验室制取二氧化碳,选取的发生装置是______。 (2)实验室制取二氧化碳的化学方程式为________________。 (3)E中观察到的现象是________。 |
查看答案和解析>>
科目: 来源:北京市门头沟区2018届九年级一模化学试卷 题型:简答题
如图为测定空气中氧气体积分数的实验装置

(1)红磷燃烧的化学方程式为_________。
(2)红磷熄灭,装置冷却到室温后,打开止水夹,观察到的现象是________。
4P+5O2 点燃 2P2O5 烧杯中的水沿导管进入集气瓶,且瓶中液面上升约到刻度1处 【解析】本题考查了测定空气中氧气含量的实验。熟练掌握实验过程、注意问题、会分析实验现象得出结论是解答本题关键。 (1)磷与氧气在点燃的条件下反应生成五氧化二磷,化学方程式为:4P+5O22P2O5; (2)由于红磷与氧气反应生成五氧化二磷固体,消耗了瓶内的气体,压强减小,打开止水夹后观察到的现...查看答案和解析>>
科目: 来源:北京市门头沟区2018届九年级一模化学试卷 题型:科学探究题
用下图所示装置,分别对燃烧条件进行研究。
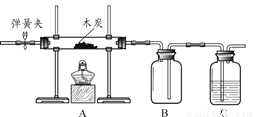
内容 | 研究燃烧条件 |
步骤 | ①打开弹簧夹,通入一段时间N2,关闭弹簧夹,加热木炭。 ②停止加热,冷却后打开弹簧夹,通入O2。 |
③加热木炭。 ④停止通O2、熄灭酒精灯。 |
(1)木炭充分燃烧时,发生反应的化学方程式为___________。
(2)步骤②的目的是_____________。
C+O2 点燃 CO2 研究燃烧温度需要达到着火点 【解析】本题考查了燃烧条件的探究。 (1)碳与氧气在点燃条件下反应生成二氧化碳,该反应的化学方程式为:C+O2 CO2; (2)步骤②停止加热,冷却后打开弹簧夹,通入O2,的目的是研究燃烧温度需要达到着火点。查看答案和解析>>
科目: 来源:北京市门头沟区2018届九年级一模化学试卷 题型:科学探究题
化学小组的同学用下图所示装置进行如下实验,实验前K1、K2、K3均为关闭状态。

内容 步骤 | 实验步骤 |
实验1 | B、C中分别盛有无色酚酞试液,打开K1,从分液漏斗中加入浓氨水,关闭K1,然后打开K2、K3。 |
实验2 | A中盛满CO2,B中盛有氢氧化钙溶液,C中盛有稀盐酸。 ①打开K1,从分液漏斗慢慢放入适量的氢氧化钠溶液,关闭K1。 ②一段时间后打开K2,观察到有A中有沉淀产生时,迅速关闭K2。 ③再打开K3,观察到A中有气泡产生。 |
(1)实验1中,可以观察到的现象是__________。
(2)实验2中,步骤①中所发生反应的化学方程式为____________________。
(3)实验2中,请解释步骤③产生气泡的原因为____________________。
B、C中的无色酚酞依次变红 2NaOH+CO2 == Na2CO3+H2O A中压强减小,C中稀盐酸沿导管进入A中,与碳酸盐发生反应。 【解析】本题考查了二氧化碳、酸碱盐的性质及化学方程式的书写,理解由于化学反应而引起装置内压强的改变是解题的关键。 (1)实验1:浓氨水具有挥发性,会发出氨气,分别进入BC两瓶,溶于水形成氨水,氨水显碱性,使无色酚酞依次变红; (2)实验2中,步骤...查看答案和解析>>
科目: 来源:北京市门头沟区2018届九年级一模化学试卷 题型:科学探究题
如图的加热袋常用于野外加热食物。加热袋中的固体粉末含镁粉、铁粉和氯化钠,使用时向其中加入水袋中的水,即可产生大量热。实验小组针对放热过程中的反应原理展开探究。


【查阅资料】
常温下镁粉能与水发生置换反应,且放热。
【进行实验】
同学们用下图所示装置进行模拟实验:分别取不同成分的固体粉末放入甲中,通过分液漏斗向其中均加入8 mL水,读取甲中所得固液混合物的最高温度,实验记录如下表:

(实验时的室温为22.8℃)
实验序号 | A | B | C | D | E | F |
固体成分 | Mg | Fe | Mg+Fe | Mg+NaCl | Fe+NaCl | Mg+Fe+NaCl |
乙中现象 | 少量肥皂泡,难以点燃 | ______ | 少量肥皂泡,难以点燃 | 较多肥皂泡,点燃有爆鸣声 | 无肥皂泡 | 大量肥皂泡,点燃有爆鸣声 |
混合物温度 | 23.1℃ | 22.8℃ | 23.1℃ | 24.2℃ | 22.8℃ | 27.2℃ |
【解释与结论】
(1)实验B,乙中现象为_______________。
(2)实验A证明了镁粉与水能反应,完成该反应的化学方程式Mg+2H2O=____+H2  。
。
(3)使镁粉与水迅速反应并放热的最佳方法是向镁粉中加入_____________。
【反思改进】
(4)同学们分析实验数据发现,升高的温度没有达到食品加热袋的效果,其可能的原因是___________。
(5)同学们根据实验结果进一步猜测,实验F中的反应结束后,甲中剩余固体混合物中仍然含有铁粉,检验其铁粉存在的的实验方案为:取少量固体混合物________。
(6)从上述实验初步得出“NaCl溶于水没有热量的变化”的结论,依据的两个实验是(填实验序号)______________。
无肥皂泡 Mg(OH)2 铁粉 食盐 没有保温措施,热量散失 加入稀盐酸,有气泡产生,溶液变浅绿色,证明有铁粉 B E 【解析】本题考查了实验探究物质的性质或变化规律,化学方程式的书写。通过实验资料和实验分析,得到了正确的结论,要具体分析,综合掌握。 (1)铁不能与水反应,铁和水混合时,无肥皂泡产生; (2)根据化学方程式,反应前镁原子、氢原子、氧原子的数目分别为1、4、2,反应...查看答案和解析>>
科目: 来源:广西贵港市平南县2018届九年级第二次模拟考试化学试卷 题型:单选题
下列物质的性质中,属于化学性质的是
A. 干冰易升华 B. 浓盐酸易挥发 C. 氢气可燃烧 D. 氢氧化钠固体易潮解
C 【解析】A、干冰易升华不需要通过化学变化就能表现出来,属于物理性质,错误;B、浓盐酸易挥发不需要通过化学变化就能表现出来,属于物理性质,错误;C、氢气可燃烧需要通过氢气和氧气反应生成水才能表现出来,属于化学性质,正确;D、氢氧化钠固体易潮解不需要通过化学变化就能表现出来,属于物理性质,错误。故选C。查看答案和解析>>
科目: 来源:广西贵港市平南县2018届九年级第二次模拟考试化学试卷 题型:单选题
为了达到相应的实验目的,下列实验设计不合理的是
A.  分离H2O2和MnO2制O2后的固液混合物
分离H2O2和MnO2制O2后的固液混合物
B.  除去CO中的CO2气体
除去CO中的CO2气体
C.  区分NaCl、NH4NO3、NaOH三种固体
区分NaCl、NH4NO3、NaOH三种固体
D.  探究可燃物燃烧的条件
探究可燃物燃烧的条件
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com