
科目: 来源:江苏省南通市海安县2018届九年级学业水平测试化学试卷 题型:单选题
X、Y、Z3种固体物质(不含结晶水)的溶解度曲线如图所示。下列说法中错误的是

A. t2℃时,3种物质的溶解度的大小关系为Y>Z=X
B. X中含有少量Z,可以采用降温结晶的方法提纯X
C. 将溶质质量分数为25%的X溶液从t3℃降温到t1℃时,所得溶液中溶质的质量分数为20%
D. t3℃时,向盛有等质量X、Y、Z固体的3只烧杯中分别加水配成饱和溶液,所得溶液的质量大小为X>Y>Z
D 【解析】A、由溶解度曲线可知,t2℃时,3种物质的溶解度的大小关系为Y>Z=X,正确;B、由溶解度曲线可知,X的溶解度随温度的升高而增大,且受温度的影响变化较大。Z的溶解度随温度的升高而减小。故X中含有少量Z,可以采用降温结晶的方法提纯X,正确;C、由图可知,t1℃时,X的溶解度为25g,那么该温度下饱和溶液溶质质量分数=×100%=20%,故将溶质质量分数为25%的X溶液从t3℃降温到...查看答案和解析>>
科目: 来源:江苏省南通市海安县2018届九年级学业水平测试化学试卷 题型:单选题
下列物质的提纯所用试剂和主要实验操作均正确的是
选项 | 物质(括号内为杂质) | 所用试剂 | 主要实验操作 |
A | MnO2(KCl) | 水 | 溶解、过滤、蒸发、结晶 |
B | CaCl2溶液(HCl) | 适量Na2CO3固体 | 溶解 |
C | CO(CO2) | 浓氢氧化钠溶液、浓硫酸 | 洗气、干燥 |
D | Cu(CuO) | O2 | 加热 |
A. A B. B C. C D. D
C 【解析】A、MnO2不溶于水,KCl易溶于水,将其溶解、过滤、洗涤、干燥即可,错误;B、碳酸钠与氯化钙溶液反应,违背除杂原则,错误;C、一氧化碳不与浓氢氧化钠溶液反应,也不与浓硫酸反应。二氧化碳与浓氢氧化钠溶液反应生成碳酸钠和水,再通过浓硫酸干燥,正确;D、铜与氧气在加热的条件下反应生成氧化铜,违背除杂原则,错误。故选C。查看答案和解析>>
科目: 来源:江苏省南通市海安县2018届九年级学业水平测试化学试卷 题型:单选题
推理是一种重要的化学思维方法,以下推理正确的是
A. 某盐能解离出金属离子和酸根离子,则该盐的组成中含非金属元素
B. 某物质在氧气中燃烧生成CO2和H2O,则该物质含有C、H、O三种元素
C. CaO能与H2O反应生成Ca(OH)2,则CuO能与H2O反应生成 Cu(OH)2
D. 二氧化碳能使燃着的木条熄灭,则能使燃着木条熄灭的气体一定是二氧化碳
A 【解析】A、盐是由金属离子和酸根离子构成的化合物,酸根离子由非金属元素构成,正确;B、某物质在氧气中燃烧生成CO2和H2O,则该物质一定含有C、H元素,可能含有O元素,错误;C、CaO能与H2O反应生成Ca(OH)2,但CuO不能与H2O反应生成 Cu(OH)2,错误;D、二氧化碳能使燃着的木条熄灭,但能使燃着木条熄灭的气体不一定是二氧化碳,如氮气,错误。故选A。查看答案和解析>>
科目: 来源:江苏省南通市海安县2018届九年级学业水平测试化学试卷 题型:单选题
下列图示实验能达到对应目的的是
A.  测定空气中O2的含量
测定空气中O2的含量
B. 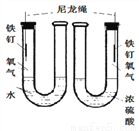 探究铁的生锈与水有关
探究铁的生锈与水有关
C. 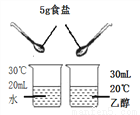 探究溶剂种类对物质溶解性的影响
探究溶剂种类对物质溶解性的影响
D.  鉴别NH4Cl和NH4NO3溶液
鉴别NH4Cl和NH4NO3溶液
查看答案和解析>>
科目: 来源:江苏省南通市海安县2018届九年级学业水平测试化学试卷 题型:单选题
一定条件下,在一个密闭容器内发生某反应,测得反应前后各粒子的数目如下表所示.
粒子种类 |
|
|
|
|
|
反应前的数目 | 2n | 7n | 0 | x | |
反应后的数目 | 0 | n | 4n | 7n |
以下有关说法中,正确的是
A. 表中x=3n
B. 由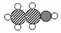 构成的物质属于无机化合物
构成的物质属于无机化合物
C. 由 构成的物质中,
构成的物质中, 对应元素的含量约为72.7%
对应元素的含量约为72.7%
D. 由 与
与 构成的对应物质,在该反应中的质量比为16:9
构成的对应物质,在该反应中的质量比为16:9
查看答案和解析>>
科目: 来源:江苏省南通市海安县2018届九年级学业水平测试化学试卷 题型:填空题
请运用所学化学知识填空:
(1)拉瓦锡通过实验测得,氧气约占空气体积的________;硫在氧气燃烧会伴随___________色火焰。
(2)从微观视角看,“春雨丽润泽桃花开,微风拂面清香来”说明_________; CH3COOH、HCl等物质的水溶液都能使石蕊溶液变为红色的原因是:它们的溶波中都含有_________(填微粒名称)。
(3)构成硫酸铁的阳离子符号为:_________;甲烷完全燃烧的化学方程式为:___________________。
(4)依据下图回答问题:
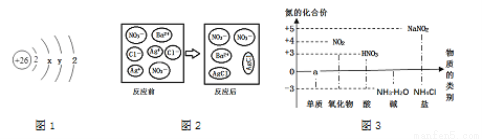
①图1中y的值为________
②另写1个与图2所示微观反应本质相同的化学方程式_____________·
③写出图3中a处的1种物质名称:_____________,其中位置放错的物质有:___________(填化学式)。
1/5 蓝紫 构成物质的微粒是不断运动的 氢离子 Fe3+ CH4 + 2O2 CO2 +2H2O 14 NaCl + AgNO3 = AgCl ↓+ NaNO3 氮气 HNO3、NaNO2 【解析】(1)根据氧气约占空气体积的五分之一解答;根据硫在氧气燃烧产生蓝紫色火焰解答;(2)根据构成物质的微粒是不断运动的解答;根据能使石蕊溶液变为红色的物质显酸性,酸性物质中含有氢离子解答;(3)根据...查看答案和解析>>
科目: 来源:江苏省南通市海安县2018届九年级学业水平测试化学试卷 题型:流程题
锰是治炼工业中常用的添加剂。以碳酸锰矿(主要成分为MnCO3,还含有 FeCO3、NiCO3等杂质)为原料生产金属锰的工艺流程如下图,请回答以下问题:
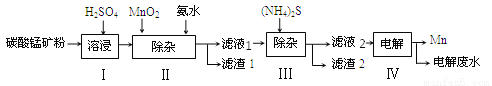
(1)步骤Ⅰ中,将碳酸锰矿研磨成粉末的主要目的是_______,其中碳酸锰与硫酸反应的化学方程式为_________________。
(2)步骤Ⅱ中,先加入二氧化锰发生以下反应:MnO2+2FeSO4+2H2SO4=MnSO4+2H2O+x,x的化学式为______;已知滤液1中的主要溶质为MnSO4同时还含有少量NiSO4,则步骤Ⅱ中加入氨水的主要目的是________。
(3)步骤Ⅲ中,所得滤液2中含有的溶质为MnSO4、(NH4)2SO4,则滤渣2中主要成分为______(填化学式)
(4)步骤Ⅳ中,电解后的废液中还含有Mn2+,常用石灰乳进行一级沉降得到沉淀Mn(OH)2和氨气,过滤后,再向滤液中加入Na2S进行二级沉降得到沉淀MnS。写出二级沉降过程中发生的化学反应方程式:___________________;沉降过程的产物中,______________________可循环利用于上述流程。
增加反应物之间的接触面积,使反应更充分,同时加快反应速率 MnCO3 + H2SO4 = MnSO4 + H2O + CO2 ↑ Fe2(SO4)3 除去铁离子 NiS MnSO4+ Na2S = Na2SO4 + MnS↓ 氨气 【解析】(1)根据将碳酸锰矿研磨成粉末的主要目的是增加反应物之间的接触面积,使反应更充分,同时加快反应速率解答;根据碳酸锰与硫酸反应生成硫酸锰、水、二氧化碳解答;...查看答案和解析>>
科目: 来源:江苏省南通市海安县2018届九年级学业水平测试化学试卷 题型:简答题
请结合所学化学知识回答以下问题:
(1)下图为中国自主研制的新一代战斗机,其中机翼前后缘采用了玻璃纤维增强塑料(玻璃钢),机轮由轮毂和轮胎组成,驾驶座盖和挡风玻璃采用了两烯酸酯透明塑料,其中玻璃纤维增强塑料属于____(填字母)

a.金属材料 b.合成材料 C.复合材料
(2)现代喷气式战斗机所用燃料是航空煤油。加热炼制_______(填1种化石燃料名称).可以获得航空煤油等不同的产品,不同类型的发动机选用的燃料不同,氢动汽车采用氢气作燃燃料,目前在生活中大量使用氢能源还存在诸多围难(如,制氢成本高)。在实验室里,制取氢气的化学反应方程式为________。
(3)为保障飞行员的健康体魄,后勤部门为他们提供的主食是易于消化的面包、米饭等食物,这些食物中富含________(填1种基本营养素),同时建议他们平时多饮用富硒茶水,属于人体必需的______(填“微量”或“常量”)元素。
(4)新一代战斗机机翼翼梁采用了特种合金,工业上生产该合金的反应为:TiCl4+2Mg高温Ti+2MgCl2,该反应中_________(填微粒的符号)得到了电子,反应的基本类型是:____________。
复合材料 石油 Zn+H2SO4= ZnSO4+H2↑ 糖类 微量 Ti4+ 置换反应 【解析】(1)根据玻璃钢属于复合材料解答;(2)根据航空煤油是石油炼制产品解答;根据锌与硫酸反应生成硫酸锌和氢气解答;(3)根据面包、米饭中富含糖类解答;根据硒属于微量元素解答;(4)根据得到电子化合价降低分析解答。(1)玻璃纤维增强塑料(玻璃钢)属于复合材料;(2)航空煤油是石油炼制产品;锌与硫酸反应生...查看答案和解析>>
科目: 来源:江苏省南通市海安县2018届九年级学业水平测试化学试卷 题型:综合题
下图是“研究燃烧条件”的实验装置,请回答实验内容中的相关问题:
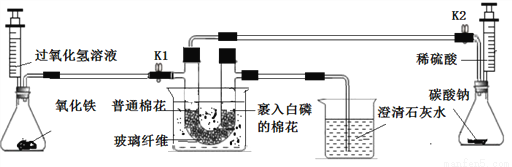
实验准备:连接仪器,______,将充足的药品装入装置A、B、C、D中,盛装氧化铁的玻璃仪器名称为______
实验步骤1:将U形管放入冰水中,打开K1,关闭K2,向U形管充入氧气,两端的棉花都没有燃烧。此时装置A中发生的化学反应方程式为________________。
实验步骤2:关闭K1,打开K2,先从U形管左端通入气体,待观察到表明氧气已排尽,再将U形管放入的80℃的热水中,此时两端棉花也都没有燃烧。表明氧气已排尽的实验现象是______________,产生该现象的化学反应方程式为_________________。
实验步骤3:打开K1,关闭K2,从U形管左端通入氧气。右端裹入白磷的疏松棉花团先冒白烟,片刻后棉花开始燃烧,左端的棉花团仍然没有发生变化。实验步骤1和实验步骤3中对比研究的变量是________。白磷燃烧过程中伴随的能量变化是:_____________。
实验步骤4:在步骤3棉花燃烧的过程中, ____________________(填具体操作和实验现象)。该步骤也能说明燃烧需要氧气,同时说明二氧化碳具有________________________的性质。
实验推算:若以上实验中共需要使用330mL二氧化碳(已知:二氧化碳的密度为2g/L),则实验前至少需要向装置D中加入________g(结果保留2位小数)碳酸钠钠固体。
检查装置的气密性 锥形瓶 2H2O2氧化铁2H2O+O2 装置C中烧杯内的澄清石灰水变浑浊 CO2+Ca(OH)2 =CaCO3 ↓+ H2O 温度 化学能转化为热能 关闭K1,打开K2,从U形管左端通入CO2(1分),右端燃烧的棉花很快熄灭 既不燃烧也不支持燃烧 1.59 【解析】实验准备:根据装入药品前应检查装置的气密性解答;根据常见仪器解答;实验步骤1:根据过氧化氢溶液在氧化铁的催化下...查看答案和解析>>
科目: 来源:江苏省南通市海安县2018届九年级学业水平测试化学试卷 题型:计算题
为测定某部分变质氢氧化钠固体中氢氧化钠的含量,研究性学习小组称取42.4g干燥的圆体样品并将其配制成1000mL溶液,分别取出100mL溶液用2种方法进行了测定。
方法1:向100mL样品中加入过量的浓盐酸,并用足量氢氧化钠溶液吸收产生的气体,称得浓氢氧化钠溶液增加了1.10g
方法2:向100mL样品中加入过量BaCl2液,经过滤、洗涤、干燥等操作,分离出反应生成的沉淀物,称得其质量为3.94g
(1)请选用合理方法采集的数据求解固体中氢氧化钠的质量分数为________。(写出计算过程)
(2)向上述用剩的溶液中加入________gBa(OH)2固体,过滤,则可获得纯净的氢氧化钠溶液。(结果保留2位小数)
50% 27.36 【解析】(1)根据氢氧化钠变质生成碳酸钠,碳酸钠与氯化钡反应生成碳酸钡沉淀结合反应的化学方程式计算解答;(2)根据反应的化学方程式计算解答。(1)设100mL样品中碳酸钠的质量为x。 Na2CO3+ BaCl2=BaCO3↓+2NaCl 106 197 x 3.94g x=2.12g 则1000mL溶液中碳酸钠的质量=2.12g×(1000m...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com